题目内容
在25度时,纯水中C(H+).C(OH-)=分析:25℃时纯水中c(H+)=c(OH-)=10-7mol/L;溶液酸碱性取决c(H+)与c(OH-)的相对大小,25℃酸性溶液中c(H+)>c(OH-),25℃Kw=10-14,故c(H+)>10-7mol/L,根据PH=-logc(H+)判断.
解答:解:25℃时纯水中c(H+)=c(OH-)=10-7mol/L,所以c(H+)?c(OH-)=10-14;
溶液酸碱性取决c(H+)与c(OH-)的相对大小,25℃酸性溶液中c(H+)>c(OH-),25℃Kw=10-14,故c(H+)>10-7mol/L;
根据PH=-logc(H+),c(H+)>10-7mol/L,所以PH<-log10-7=7.
故答案为:10-14;大于;小于.
溶液酸碱性取决c(H+)与c(OH-)的相对大小,25℃酸性溶液中c(H+)>c(OH-),25℃Kw=10-14,故c(H+)>10-7mol/L;
根据PH=-logc(H+),c(H+)>10-7mol/L,所以PH<-log10-7=7.
故答案为:10-14;大于;小于.
点评:考查水的离子积、溶液酸碱性、PH值计算等,比较基础,注意溶液酸碱性取决c(H+)与c(OH-)的相对大小,中性溶液的PH值可以小于7.

练习册系列答案
相关题目
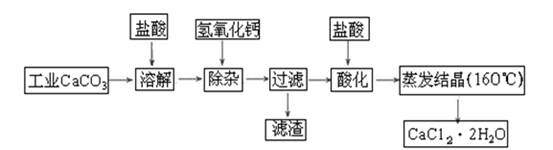 (1)除杂操作是加入氢氧化钙固体,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+,检验Fe(OH)3是否沉淀完全的实验操作是_____________________________________
(1)除杂操作是加入氢氧化钙固体,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+,检验Fe(OH)3是否沉淀完全的实验操作是_____________________________________
 ______________,
______________, 11mol3·L-3,求该温度下饱和的Mg(OH)2溶液的pH为 。
11mol3·L-3,求该温度下饱和的Mg(OH)2溶液的pH为 。 H++OH-,在25℃、35℃时其离子积分别为
H++OH-,在25℃、35℃时其离子积分别为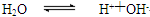 ,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述中正确的是
,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述中正确的是