题目内容
3.我国化工专家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如图1: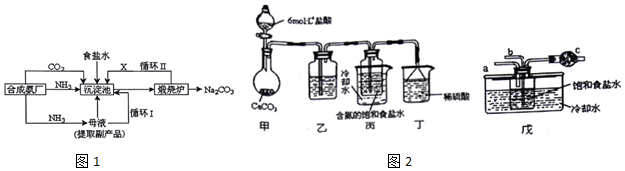
(1)沉淀池中发生的化学反应方程式是NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓.
(2)上述流程中X物质的分子式CO2.
(3)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是C (选填字母).
A.碳酸氢钠难溶于水
B.碳酸氢钠受热易分解
C.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(4)某探究活动小组根据上述制碱原理,欲制备碳酸氢钠,同学们按各自设计的方案进行实验.第一位同学:将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如图2所示(图中夹持、固定用的仪器未画出).
请回答:
①甲中发生反应的离子方程式是CaCO3+2H+=Ca2++H2O+CO2↑
②乙装置中的试剂是饱和碳酸氢钠溶液
③实验结束后,分离出NaHCO3 晶体的操作是过滤(填分离操作的名称).
第二位同学:用图中戊装置进行实验(其它装置未画出).
④为提高二氧化碳在此反应液中被吸收的程度,实验时,须先从a管通入NH3 气体,再从b管通入CO2 气体.
⑤装置c中的试剂为C (选填字母)
A.碱石灰 B.浓硫酸 C.无水氯化钙
(5)请你再写出一种实验室制取少量碳酸氢钠的方法:(用简要的文字和相关的化学反应方程式来描述):NaOH+CO2=NaHCO3或Na2CO3+CO2+H2O=2NaHCO3.
分析 将二氧化碳和氨气、食盐水加入沉淀池中,发生的反应为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,得到的沉淀在煅烧炉中发生反应2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2,从而得到Na2CO3,煅烧过程中得到的X为CO2要循环利用,母液中含有的铵根离子和碱反应得到的氨气也能循环利用,
(1)沉淀池中氯化钠、二氧化碳、氨气和水发生复分解反应生成碳酸氢钠和氯化铵;
(2)煅烧过程中得到的X为CO2要循环利用;
(3)依据题干中信息碳酸氢钠溶解度相对较小分析判断;
(4)①装置甲中碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,据此写出反应的化学方程式;
②依据用盐酸制取二氧化碳时常会含有氯化氢气体分析即可解答;
③依据分离固体与液体采用的实验操作分析解答;
④根据氨气易溶于水,判断通入氨气的导管不能插入溶液中,再根据二氧化碳的溶解度较小,为了提高二氧化碳的利用率,应该先通入氨气进行解答
⑤防止NH3污染空气;
(5)氢氧化钠与过量的二氧化碳反应生成碳酸氢钠,也可以用碳酸钠与二氧化碳反应生成碳酸氢钠,据此写出反应的化学方程式.
解答 解:(1)沉淀池中发生的化学反应为饱和食盐水中通入氨气和二氧化碳析出碳酸氢钠晶体,反应方程式为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓,故答案为:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓;
(2)在联合制碱法中二氧化碳是反应的原料同时也是反应的副产物,可以循环利用,故答案为:CO2;
(3)A.碳酸氢钠易溶于水,故A错误;
B.碳酸氢钠受热易分解,与其在溶液中首先结晶析出无关,故B错误;
C.碳酸氢钠的溶解度相对于氯化铵来说碳酸氢钠的溶解度更小一些,所以在溶液中首先结晶析出,故C正确,
故答案为;C;
(4)①装置甲发生的反应方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
②利用盐酸制取二氧化碳时,因盐酸易挥发,所以二氧化碳中常会含有氯化氢气体,碳酸氢钠能与盐酸反应不与二氧化碳反应,所以通过碳酸氢钠的溶液是可以除掉二氧化碳气体中的氯化氢气体,故答案为:饱和碳酸氢钠溶液;
③分离出NaHCO3晶体的操作是分离固体与液体,常采用的实验操作是过滤操作,故答案为:过滤;
④制取碳酸氢钠时先要得到含氨的饱和食盐水,氨气极易溶于水,通入氨气的导管不能直接插入溶液中,所以导管a通入氨气,导管b通入二氧化碳;由于二氧化碳在水中溶解度减小,为了保证了从b通入二氧化碳时二氧化碳被充分反应,应该先通入氨气,再通入二氧化碳,故答案为:NH3(氨);CO2(二氧化碳);
⑤NH3污染空气,用盛装无水CaCl2的干燥管吸收,故答案为:C;
(5)可以将过量的CO2通入NaOH溶液或Na2CO3中,反应的化学方程式为:NaOH+CO2=NaHCO3或Na2CO3+CO2+H2O=2NaHCO3,
故答案为:NaOH+CO2=NaHCO3或Na2CO3+CO2+H2O=2NaHCO3.
点评 本题考查了纯碱工业原理及其应用,题目难度中等,明确制备流程及常见物质的性质为解答关键,注意掌握侯氏制碱法的反应原理,试题侧重考查学生的分析、理解能力及化学实验能力.

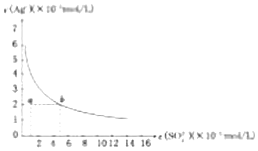
| A. | 在SO42-浓度为3mol/L的溶液中肯定不存在Ag+ | |
| B. | 0.02mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合不会生成沉淀 | |
| C. | 在任何存在Ag2SO4的悬浊溶度积中c(Ag+)=2c(SO42-) | |
| D. | a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
| t/min | 1 | 2 | 3 | 4 |
| c(N2O5)/mol.L-1 | 0.133 | 0.080 | 0.057 | 0.040 |
| v正/mol.L-1.min-1 | 0.0466 | 0.028 | 0.020 | 0.014 |
(1)该速率表达式中,m=1,k正=0.35min-1.
(2)若某时刻c(N2O5)=0.100mol•L-1,则v正≈0.035mol.L-1.min-1.
(3)第4min时,该可逆反应v正≥(填“>”“<”或“=”或“≥”)v逆.
①它们所含的分子数目之比为1:1 ②它们所含的O原子数目之比为1:2 ③它们所含的原子数目之比为2:3 ④它们所含的C原子数目之比为1:1 ⑤它们所含的电子数目之比为7:11.
| A. | ①②④ | B. | ①②③ | C. | ①②③⑤ | D. | 全部正确 |
| A. | Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同 | |
| B. | Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同 | |
| C. | 达平衡时,Ⅰ途径的反应速率v1等于Ⅱ途径的反应速率v2 | |
| D. | 达平衡时,Ⅰ途径混合气体的密度与Ⅱ途径混合气体的密度相等 |
| A. | 泡沫灭火器利用Al3+、HCO3-相互反应可放出二氧化碳气体 | |
| B. | 使用热的纯碱水洗手时更容易除去手上的油脂污垢 | |
| C. | 明矾能用于净水 | |
| D. | 铜绿的生成 |
| A. | OH-、H2O、F- | B. | NH3、NH4+、NH2- | C. | H3O+、NH4+、NH2- | D. | HCl、F2、H2S |
| A. | 离子化合物都能溶于水,而共价化合物都不溶于水 | |
| B. | 离子化合物的熔点一般较高,而共价化合物的熔点一般较低 | |
| C. | 离子化合物的硬度一般较大,而共价化合物的硬度一般较小 | |
| D. | 离子化合物在熔融条件下能够导电,而共价化合物在熔融条件下不能导电 |
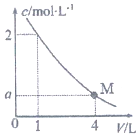 如图是BaC12溶液在稀释过程中,c(Ba2+)随溶液体积的变化曲线图,则M点时,溶液中c(Cl-)为( )
如图是BaC12溶液在稀释过程中,c(Ba2+)随溶液体积的变化曲线图,则M点时,溶液中c(Cl-)为( )| A. | 0.25mol/L | B. | 0.5mol/L | C. | 1 mol/L | D. | 2mol/L |