��Ŀ����
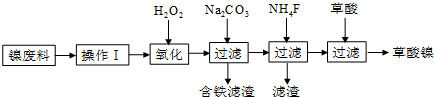
15������ͼ1��ʾװ�ÿ������һϵ��ʵ�飨ͼ�мг�װ������ȥ����
��װ��A��Ũ�����Ũ��������ȡHCl���壬װ��B�е������������������´�����
�ٰ���ij�������ʣ���պ��KI��Һ����պ��ʯ����Һ
��ش��������⣺
��1������P�������Ƿ�Һ©����
��2���ٴ����е�ij�������ʿ����� ������ţ�b��
a��MnO2 b��KMnO4 c��KCl d��Cu
��Ӧ��ʼ�۲쵽�ڴ����ػ�ɫ���ʲ�����д���ڴ�������Ӧ�����ӷ���ʽCl2+2I-�TI2+2Cl-��
��3����ʵ������У��ڢ۴��ܹ۲쵽�ȱ�����ɫ��
��4����ͬѧΪ����֤ʣ���������Ҫ�ɷ֣���C���������ͼװ�ã�D��װ��ͭ˿����װ��E���Թ��в����κ��Լ���װ��F���ձ��м���������AgNO3��Һ
��ʵ������У�װ��D����������֤ʣ�������к���������
��װ��F�е��������а�ɫ����������
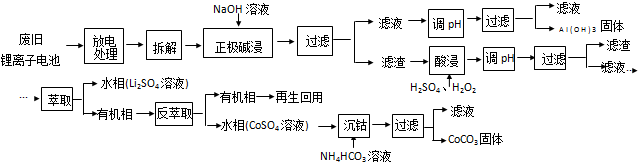
����ͬѧ��Ϊ��ͬѧ��ʵ����ȱ�ݣ�Ϊ��ȷ��ʵ��Ŀɿ��ԣ���ͬѧ�����E��F����װ����ĸ��֮���װ��ͼ3��ʾװ�ã�
����Ϊ��ͼ3���ƿ�пɼ�������AC������ĸ���ţ���
A�����۵⻯����Һ B�����Ȼ�̼��Һ
C��ʪ�����ɫ���� D������ʳ��ˮ��
���� װ��A����Ũ�����Ũ��������ȡHCl���壬��Ũ����ϡ��ʱ������������ʹ�����е��Ȼ�������ӷ����Ȼ��⣬����Ӧ��Ũ���Ỻ�����뵽Ũ�����У�װ��B����ͨ���ٺ�������Cl2��KMnO4����HCl�õ�Cl2��KMnO4+16HCl�T2KCl+2MnCl2+5Cl2��+8H2O����պ��KI��Һ�����ػ�ɫ����ȷ��Ϊ���ʵ⣬��������⻯�ط�Ӧ���ɵ��ʵ⣬����ʽΪ��Cl2+2KI=2KCl+I2����պ��ʯ����Һ��Cl2����ˮ��Ӧ����HCl��HClO��HCl�������ԣ���ʹʯ����Һ��죬HClO����ǿ��������ʹ��ɫ��ȥ��
��1�������������������䳣�����������ƽ��
��2����ͨ���ٺ�������Cl2��KMnO4������HCl�õ�Cl2�����ػ�ɫ����ȷ��Ϊ���ʵ⣬�����������������ɵⵥ�ʣ�
��3��Cl2����ˮ��Ӧ����HCl��HClO��HCl�������Ժ�HClO����ǿ�����ԣ�
��4����ʣ���������Ҫ�ɷ֣�����Ϊ�������Ȼ�������ߵĻ���ʵ������У��۲쵽װ��D�����ػ�ɫ���ʲ�������֤ʣ�������к���������
��װ��F���ձ��м�������AgNO3��Һ�������Ӻ������ӷ�Ӧ���Ȼ�����
�������е�������ͭ��Ӧ��ʣ�࣬ͨ��Fװ����Ҳ�������Ȼ�����ɫ������Ӱ���Ȼ���ļ��飬��Ҫ��ͨ����������Һǰ�����Ƿ��������Ĵ��ڣ����ƿ���Լ��������������������ԣ�ѡ����۵⻯����Һ��Ҳ���Է���ʪ�����ɫ����������������ˮ��Ӧ�Ĵ������Ư���Խ��з�����֤�����Դ��Լ�������Ϊ�����Ȼ��������е��������ų�����Ӱ���Ȼ���ļ��飮
��� �⣺��1������P�����������������в���������Ϊ��Һ©����
�ʴ�Ϊ����Һ©����
��2����ͨ���ٺ�������Cl2����KMnO4��Һ������HCl�õ�Cl2�����Ԣٴ����е�ij�������ʿ�����KMnO4�����ػ�ɫ����ȷ��Ϊ���ʵ⣬±�ص��ʼ��ܷ����û���Ӧ��Cl2+2KI=2KCl+I2����Ӧ�����ӷ���ʽΪ��Cl2+2I-�TI2+2Cl-��
�ʴ�Ϊ��b�� Cl2+2I-�TI2+2Cl-��
��3����Cl2����ˮ��Ӧ����HCl��HClO��HCl�������ԣ���ʹʯ����Һ��죬HClO����ǿ��������ʹ��ɫ��ȥ��
�ʴ�Ϊ���ȱ�����ɫ��
��4����ʣ���������Ҫ�ɷ֣�����Ϊ�������Ȼ�������ߵĻ����Ȼ�����ͭ����Ӧ��ͭ��������Ӧ�����ػ�ɫ���Ȼ�ͭ����ʣ�������к���������ʵ������У�װ��D���ػ�ɫ�̶�������
�ʴ�Ϊ����֤ʣ�������к���������
��ʣ���������Ҫ�ɷ֣�����Ϊ�������Ȼ�������ߵĻ�������ˮ��ˮ�к��������ӣ������Ӻ������ӷ�Ӧ��Ag++Cl-=AgCl�����а�ɫ����������
�ʴ�Ϊ���а�ɫ����������
����ͬѧ��Ϊ��ͬѧ��ʵ����ȱ�ݣ�����֤������ͨ��AgNO3��Һ�������в��������������е�������ͭ��Ӧ��ʣ�࣬ͨ��Fװ����Ҳ�������Ȼ�����ɫ������Ӱ���Ȼ���ļ��飬��Ҫ��ͨ����������Һǰ�����Ƿ��������Ĵ��ڣ����ƿ���Լ��������������������ԣ�ѡ����۵⻯����Һ��Ҳ���Է���ʪ�����ɫ����������������ˮ��Ӧ�Ĵ������Ư���Խ��з�����֤��Ϊ��ȷ��ʵ��Ŀɿ��ԣ���ͬѧ�����E��F֮���װͼ2��ʾװ���п��Էŵ��۵⻯����Һ��������ɫ֤�����������������������ʪ�����ɫ������������ɫ֤�����������ڣ�����֤�����У�BD�ޱ仯������֤��������ѡ��AC�����Լ�������Ϊ�����Ȼ��������е��������ų�����Ӱ���Ȼ���ļ��飮
�ʴ�Ϊ��E��F��AC��
���� ���⿼����ʵ�����Ʊ�������ʵ�������������֤��������֤ʵ�����Ʒ���Ӧ�ã��ܹ�����ʵ�������ж����ʵ����ʣ����ӷ�Ӧ����������ж��ǽ���ؼ�����Ŀ�Ѷ��еȣ�

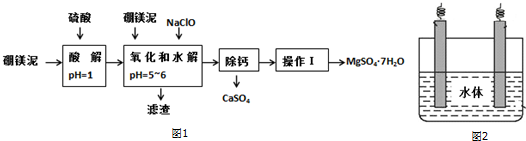
��֪��ijЩ�������������pH���±���ʾ��
| �������� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Mg��OH��2 | 9.3 | 10.8 |
| Fe��OH��2 | 7.6 | 9.6 |
| Fe��OH��3 | 2.7 | 3.7 |
| Al��OH��3 | 3.7 | 4.7 |
��1�����������У����ӿ����ʱ�Ļ�ѧ��Ӧ���ʣ���������ֿ��еĴ�ʩ���ʵ����¡�����þ����顢����衢���ʵ���������Ũ�ȣ�
��2�������NaClO����Mn2+��Ӧ��Mn2++ClO-+H2O=MnO2��+2H++Cl-������һ������Ҳ�ᱻNaClO������������ˮ�⣬�÷�Ӧ�����ӷ���ʽΪ2Fe2++ClO-+5H2O=2Fe��OH��3��+Cl-+4H+��
��3����������Ҫ�ɷݳ�����Fe��OH��3��Al��OH��3��MnO2�⣬����SiO2��CaSO4��
��4����֪MgSO4��CaSO4���ܽ�����±���
| �¶ȣ��棩 | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
��5��ʵ�����ṩ����þ�100g���õ���MgSO4•7H2OΪ172.2g������MgSO4•7H2O�IJ���Ϊ70%����������λ��Ч���֣�
��6������þ��������Ȼˮ���������ĵ绯ѧ���������ͼ2����ʾ��ͼ��������Ӧ��ע��
| A�� | 2Cl--2e-=Cl2�� | B�� | Cu2++2e-=Cu | ||
| C�� | 4OH--4e-=2H2O+O2�� | D�� | 2H++2e-=H2�� |

 ��
��
 ��
��