籾朕坪否
郡哘⦿CaCl2+CO2+H2O=CaCO3+2HCl壓販採秤趨和脅音嬬窟伏郡哘⇧圻咀頁乎郡哘↙ ⇄
| A、@H﹅0@S﹅0 |
| B、@H〽0@S〽0 |
| C、@H〽0@S﹅0 |
| D、@H﹅0@S〽0 |
深泣⦿貶延才贍延
廨籾⦿晒僥郡哘嶄議嬬楚延晒
蛍裂⦿郡哘徭窟序佩議登僅卆象頁@H-T@S〽0⇧潤栽郡哘蒙尢蛍裂登僅◉
盾基⦿
盾⦿郡哘⦿CaCl2+CO2+H2O=CaCO3+2HCl⇧壓販採秤趨和脅音嬬窟伏郡哘⇧@H-T@S﹅0⇧郡哘頁賑悶悶持受弌議郡哘⇧@S〽0⇧@H﹅0⇧諾怎⇧@H-T@S﹅0⇧壓販採秤趨和脅音嬬窟伏郡哘◉
絞僉D⤴
絞僉D⤴
泣得⦿云籾深臥阻晒僥郡哘徭窟序佩議登僅卆象⇧郡哘蒙尢才蛍裂卆象頁盾籾購囚⇧籾朕熟酒汽⤴

膳楼過狼双基宛
屢購籾朕
墜-蛇栽署辛壓宰郡哘均嶄喘恬犯住算匣⤴5.05g墜-蛇栽署卑噐200mL邦伏撹0.075mol狽賑⤴
↙1⇄柴麻卑匣嶄狽剳功宣徨議麗嵎議楚敵業↙策待卑匣悶持延晒⇄⤴
↙2⇄柴麻旺鳩協乎墜-蛇栽署議晒僥塀⤴
↙1⇄柴麻卑匣嶄狽剳功宣徨議麗嵎議楚敵業↙策待卑匣悶持延晒⇄⤴
↙2⇄柴麻旺鳩協乎墜-蛇栽署議晒僥塀⤴
和中侭双議窮徨蚊嶄嬬楚恷詰議頁↙ ⇄
| A、K蚊 | B、L 蚊 |
| C、M蚊 | D、N蚊 |
和双郡哘嶄憲栽H++OH-=H2O宣徨郡哘議頁↙ ⇄
| A、蓮葬磨嚥蓮葦邦 |
| B、蓮葬磨嚥狽剳晒欝卑匣 |
| C、蓮嵓磨嚥狽剳晒欝卑匣 |
| D、冦磨嚥狽剳晒鑓郡哘 |
嵎徨方才嶄徨方屢揖議圻徨X⇧凪剩宣徨Xn+宰翌嗤a倖窮徨⇧夸X議嵎楚方葎↙ ⇄
| A、2a | B、2↙a-n⇄ |
| C、n+2a | D、2↙a+n⇄ |
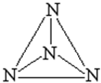 吭寄旋親僥社資誼阻自醤冩梢勺峙議N4↙蛍徨潤更泌夕侭幣⇄⇧參和嗤購麗嵎潤更議傍隈屎鳩議頁↙ ⇄
吭寄旋親僥社資誼阻自醤冩梢勺峙議N4↙蛍徨潤更泌夕侭幣⇄⇧參和嗤購麗嵎潤更議傍隈屎鳩議頁↙ ⇄| A、N譲頁參SP3墫晒⇧N-N譲葎σ囚 |
| B、N議窮減來寄噐O⇧侭參NH3議経泣詰噐H2O |
| C、N4葎圻徨唱悶⇧耽倖N議塘了方葎3 |
| D、N圻徨宰翌嗤5倖隆撹斤窮徨 |
和双光怏麗嵎⇧奉噐窮盾嵎議頁↙ ⇄
| A、NaCl |
| B、有 |
| C、宦滅 |
| D、CO2 |
和双偃峰屎鳩議頁↙ ⇄
| A、蛍盾郡哘匯協頁剳晒珊圻郡哘 |
| B、剳晒珊圻郡哘議蒙尢⦿晒栽勺窟伏延晒 |
| C、珊圻質祥頁郡哘嶄瓜珊圻議麗嵎 |
| D、壓剳晒珊圻郡哘嶄⇧払肇窮徨議圷殆晒栽勺週詰 |