题目内容
13.溶解了三种正盐的混合溶液中含有0.2molNa+、0.25molMg2+,0.4molCl-,则还含有的另一种离子SO42-为( )| A. | 0.15mol | B. | 0.3mol | C. | 0.05mol | D. | 无法计算 |
分析 溶液中阴离子和阳离子的正负电荷守恒,根据守恒思想来计算.
解答 解:溶液中阴离子和阳离子的正负电荷守恒,
即n(Na+)+2n( Mg2+)=n (Cl-)+2n(SO42-),
所以0.2 mol+2×0.25 mol=0.4 mol+2n(SO42-),
解出n(SO42-)=0.15mol.
故选:A.
点评 本题考查了溶液中阴离子和阳离子的正负电荷守恒是解决溶液中离子浓度的一种简便方法,注意灵活应用,题目较简单.

练习册系列答案
相关题目
1.2014年国家科学技术大会上,甲醇制取低碳烃技术(DMTO)获国家技术发明一等奖.DMTO主要包括煤的气化、液化、烯烃化三个阶段.
(1)煤的气化是煤在高温下转化为水煤气的过程,主要反应方程式是C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(2)煤的液化发生的主要反应如下表:
①△H1<△H2(填“>”、“<”、“=”),△H3=a+bkJ/mol(用a、b表示).
②若反应①在容积为2L的密闭容器中进行,500℃测得某一时刻体系内H2、CO、CH30H物质的量分别为4、2、10,则此时生成CH30H的速率>消耗CH30H的速率(填“>”、“<”、“=”)
③K3=2.5.
(3)烯烃化阶段:图1是烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比.图中I、II表示乙烯,III表示丙烯).
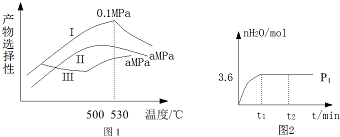
①根据图1,要尽可能多的获得乙烯,控制反应的最佳条件是530℃,0.1Mpa.
②一定温度下,某密闭容器发生如下反应:2CH3OH(g)=CH2=CH2(g)+2H2O(g),在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t1时测得甲醇的体积分数是10%,此时甲醇乙烯化的转化率是85.7%(保留3位有效数字),若要提高甲醇的转化率,可采取的措施是降低压强、分离乙烯或水(写一条即可).
③若在t2时,将容器体积迅速扩大到原来的2倍,请图2中绘制出此变化发生后至反应达到新平衡时水的物质的量与时间的关系.
(1)煤的气化是煤在高温下转化为水煤气的过程,主要反应方程式是C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(2)煤的液化发生的主要反应如下表:
| 化学反应方程式 | 平衡常数 | |
| 500℃ | 700℃ | |
| ①2H2(g)+CO(g)=CH3OH(g)△H1=akJ/mol | 2.5 | 0.2 |
| ②H2(g)+CO2(g)=CO(g)+H2O(g)△H2=bkJ/mol | 1.0 | 2.3 |
| ③3H2(g)+CO2(g)=CH3OH(g)+H2O(g)△H3 | K3 | 4.6 |
②若反应①在容积为2L的密闭容器中进行,500℃测得某一时刻体系内H2、CO、CH30H物质的量分别为4、2、10,则此时生成CH30H的速率>消耗CH30H的速率(填“>”、“<”、“=”)
③K3=2.5.
(3)烯烃化阶段:图1是烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比.图中I、II表示乙烯,III表示丙烯).

①根据图1,要尽可能多的获得乙烯,控制反应的最佳条件是530℃,0.1Mpa.
②一定温度下,某密闭容器发生如下反应:2CH3OH(g)=CH2=CH2(g)+2H2O(g),在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t1时测得甲醇的体积分数是10%,此时甲醇乙烯化的转化率是85.7%(保留3位有效数字),若要提高甲醇的转化率,可采取的措施是降低压强、分离乙烯或水(写一条即可).
③若在t2时,将容器体积迅速扩大到原来的2倍,请图2中绘制出此变化发生后至反应达到新平衡时水的物质的量与时间的关系.
8.关于HClO的分类错误的是( )
| A. | 含氧酸 | B. | 电解质 | C. | 酸性氧化物 | D. | 一元酸 |
2.下列说法中正确的是( )
| A. | 液态HCl、固态NaCl均不导电,所以HCl、NaCl均不是电解质 | |
| B. | 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质 | |
| C. | 铜、石墨均导电,所以它们是电解质 | |
| D. | NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质 |
3.生活离不开化学,下列关于生活与化学的叙述中正确的是( )
| A. | 生活中常用到的纯碱、酒精、食醋等,因都含有碳元素,所以都是有机物 | |
| B. | 有的钻戒中的钻石,是金刚石,因有正四面体的网状结构,所以硬度很大 | |
| C. | 由于啤酒中酒精含量不高,因此可以大量饮用,不会醉酒 | |
| D. | 我们用到的蔗糖、淀粉、纤维素,都是由C、H、O元素组成高分子化合物 |
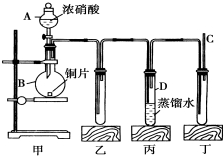 某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验.
某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验.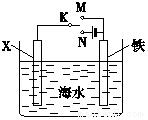 利用如图装置,可以模拟铁的电化学防护.
利用如图装置,可以模拟铁的电化学防护.