题目内容
11.水杨酸环已酯具有花香气味,可作为香精配方.其合成路线如下: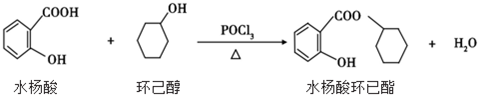
下列说法正确的是( )
| A. | 水杨酸的核磁共振氢谱有 4 个吸收峰 | |
| B. | 水杨酸、环已醇和水杨酸环已酯都能与 FeCl3 溶液发生显色反应 | |
| C. | 1mol 水杨酸跟浓溴水反应时,最多消耗 2molBr2 | |
| D. | 1mol 水杨酸环已酯在 NaOH 溶液中水解时,最多消耗 3molNaOH |
分析 A.水杨酸结构不对称,有6种不同的H;
B.环己醇不含酚羟基;
C.水杨酸中含有酚羟基,可与溴发生取代反应;
D.1mol水杨酸环己酯水解生成水杨酸,只有酚羟基和羧基与氢氧化钠反应.
解答 解:A.水杨酸结构不对称,有6种不同的H,核磁共振氢谱有6个峰,故A错误;
B.环己醇不含酚羟基,与FeCl3溶液不反应,故B错误;
C.水杨酸中含有酚羟基,邻位和对位的氢原子可被取代,最多消耗2molBr2,故C正确;
D.1mol水杨酸环己酯水解产物含有1个羧基和1个酚羟基,可与碱反应,则1mol水杨酸环己酯在NaOH溶液中水解时,最多消耗2molNaOH,故D错误;
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意把握有机物官能团的性质以及结构特点,为解答该题的关键,注意审题.

练习册系列答案
相关题目
19.下列分子中所有原子都满足最外层为8电子结构的是( )
①BeCl ②NC13 ③PCl5④COC12⑤SF6⑥XeF2⑦CS2⑧CH4⑨CF2C12⑩S2C12.
①BeCl ②NC13 ③PCl5④COC12⑤SF6⑥XeF2⑦CS2⑧CH4⑨CF2C12⑩S2C12.
| A. | ②④⑦⑧⑧⑨⑩ | B. | ②④⑦⑨⑩ | C. | ③④⑦⑩ | D. | ③④⑤⑦⑨⑩ |
6.己知亚硫酸为二元中强酸,不稳定,易被氧化请回答下列问题:
(1)下列有关亚硫酸的性质的判断正确的是abcd.
a.具有酸性 b.具有氧化性 c.具有还原性 d.有刺激性气味
(2)亚硫酸在水中电离的方程式为H2SO3?H++HSO3-,HSO3-?H++SO32-.(填标号).
(3)将亚硫酸钠溶液滴入到几种不同溶液中的现象如下表所示:
①经检验,实验I中的白色沉淀是Ag2SO3.用离子方程式解释:2Ag++SO32-=Ag2SO3↓.
②经检验,实验II中的棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-.推测反应后的溶液中一定含有溶质电离出的阴离子是SO42-、Cl-,请选用合适的试剂分别验证这些离子:取少量滤液,用足量盐酸酸化后滴加氯化钡溶液,有白色沉淀生成,证明含SO42-;另取少量滤液,用足量硝酸酸化后滴加硝酸钡溶液,过滤,向所得滤液中滴加硝酸银溶液,有白色沉淀生成,证明含Cl-.
③已知:Al2(SO3)3在水溶液中不存在,经检验,实验III中的白色沉淀中无SO42-,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色.推测沉淀中含有的阴离子为SO32-、OH-.
(1)下列有关亚硫酸的性质的判断正确的是abcd.
a.具有酸性 b.具有氧化性 c.具有还原性 d.有刺激性气味
(2)亚硫酸在水中电离的方程式为H2SO3?H++HSO3-,HSO3-?H++SO32-.(填标号).
(3)将亚硫酸钠溶液滴入到几种不同溶液中的现象如下表所示:
| 实验序号 | 试剂 | 现象 |
| I | 饱和Ag2SO4溶液 | 产生白色沉淀 |
| II | 0.2mol•L-1CuCl2溶液 | 溶液变绿,继续滴加产生棕黄色沉淀 |
| III | 0.1mol•L-1Al2(SO4)3溶液 | 开始无明显变化,继续滴加产生白色沉淀 |
②经检验,实验II中的棕黄色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-.推测反应后的溶液中一定含有溶质电离出的阴离子是SO42-、Cl-,请选用合适的试剂分别验证这些离子:取少量滤液,用足量盐酸酸化后滴加氯化钡溶液,有白色沉淀生成,证明含SO42-;另取少量滤液,用足量硝酸酸化后滴加硝酸钡溶液,过滤,向所得滤液中滴加硝酸银溶液,有白色沉淀生成,证明含Cl-.
③已知:Al2(SO3)3在水溶液中不存在,经检验,实验III中的白色沉淀中无SO42-,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色.推测沉淀中含有的阴离子为SO32-、OH-.
16.下列粒子共存的说法正确或离子方程式表达符合要求的是( )
| A. | 加入铝粉有氢气生成的溶液中可能大量存在:Ba2+、AlO2-、Cl- | |
| B. | 在含有NH3•H2O的溶液中可能大量共存的离子:Fe3+、HCO3-、NO3- | |
| C. | 亚硫酸的电离:H2SO3═HSO3-+H+ | |
| D. | 向NaHSO4溶液中加入Ba(OH)2溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
20.下列关于化学反应速率的说法正确的是( )
| A. | 化学反应速率是指一定时间内任何一种反应物浓度的减小或任何一种生成物浓度的增加 | |
| B. | 化学反应速率为“0.8 mol•L-1•s-1”所表示的意思是:时间为1 s时,某物质的浓度为0.8 mol•L-1 | |
| C. | 根据化学反应速率的大小可以知道化学反应进行的快慢 | |
| D. | 对于任何化学反应来说,反应现象越明显,反应速率越大 |

 ;
; ;
; ;
;
 )
) (其中两种)(任写两种)
(其中两种)(任写两种)