题目内容
CO和H2可作为能源和化工原料,应用十分广泛.
(1)已知:C(s)+O2(g)![]() CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g) ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)![]() 2H2O(g) ΔH2=-483.6 kJ·mol-1
2H2O(g) ΔH2=-483.6 kJ·mol-1
C(s)+H2O(g)![]() CO(g)+H2(g) ΔH3=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH3=+131.3 kJ·mol-1
则反应
CO(g)+H2(g)+O2(g)标准状况下的煤炭气
(CO、H2)336 L与氧气反应生成CO2和H2O,反应过程中转移________mol电子.(2)
熔融碳酸盐燃料电池(MCFS),是用煤气(CO+H2)作负极燃气,空气与CO2的混合气为正极助燃气,用一定比例的Li2CO3和Na2CO3低熔点混合物做电解质,以金属镍(燃料极)为催化剂制成的.负极的电极反应式为:CO+H2-4e-+2CO32-(3)
密闭容器中充有1 mol CO与2 mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)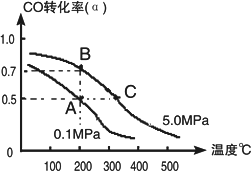
①若A、B两点表示在某时刻达到的平衡状态,此时在A点时容器的体积为10 L,则该温度下的平衡常数K=________;此时在B点时容器的体积VB________10 L(填“大于”、“小于”或“等于”).
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tC________tA(填“大于”、“小于”或“等于”).
③在不改变反应物用量情况下,为提高CO转化率可采取的措施是________.(写出两点即可)
答案:
解析:
解析:
(1)-524.8 KJ/mol 30
(2)O2+4e-+2CO2=2CO32-
(3)①100 小于
②小于
③降温、加压,将甲醇从混合体系中分离出来(答出两点即可)

练习册系列答案
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目


 CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
CH3OH(g);CO的转化率(α)与温度、压强的关系如图所示.
 CH3OH(g);CO的转化率(α)与温度、压强的关系如下图所示。
CH3OH(g);CO的转化率(α)与温度、压强的关系如下图所示。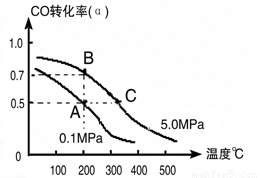
 CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如右图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如右图所示。