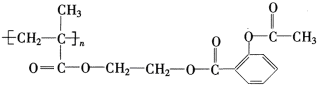题目内容
下列有关物质性质的比较中,正确的是( )
①热稳定性:CH4>NH3>H2O
②还原性:I->Br->Cl-
③酸性:H3PO4>H2SO4>HClO4
④沸点:HI>HBr>HCl>HF.
①热稳定性:CH4>NH3>H2O
②还原性:I->Br->Cl-
③酸性:H3PO4>H2SO4>HClO4
④沸点:HI>HBr>HCl>HF.
| A、①③ | B、②④ | C、①④ | D、只有② |
考点:非金属在元素周期表中的位置及其性质递变的规律,氧化性、还原性强弱的比较
专题:元素周期律与元素周期表专题
分析:①非金属性越强,气态氢化物越稳定;
②元素的非金属性越强,对应的阴离子的还原性越弱;
③元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
④HF含有氢键,沸点最高,不含氢键的氢化物,相对分子质量越大,沸点越高.
②元素的非金属性越强,对应的阴离子的还原性越弱;
③元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
④HF含有氢键,沸点最高,不含氢键的氢化物,相对分子质量越大,沸点越高.
解答:
解:①非金属性O>N>C,则气态氢化物的稳定性为CH4<NH3<H2O,故错误;
②非金属性Cl>Br>I,元素的非金属性越强,对应的阴离子的还原性越弱,故正确;
③非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故错误;
④HF含有氢键,沸点最高,应为HF>HI>HBr>HCl,故错误.
故选D.
②非金属性Cl>Br>I,元素的非金属性越强,对应的阴离子的还原性越弱,故正确;
③非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故错误;
④HF含有氢键,沸点最高,应为HF>HI>HBr>HCl,故错误.
故选D.
点评:本题考查非金属性、金属性的比较,为高频考点,侧重于学生的分析能力的考查,注意把握元素在周期表中的变化规律,题目难度不大.

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
下列有机物,既能被酸性高锰酸钾溶液氧化,又能与溴水发生加成反应的是( )
| A、苯 | B、甲苯 | C、乙烯 | D、乙烷 |
-定条件下,2SO2(g)+O2(g)?2SO2(g)△H<0.下列有关叙述正确的是( )
| A、升髙温度,v正变大,v逆变小 |
| B、恒温恒容,充入O2,02的转化率升高 |
| C、恒温恒压,充人N2,平衡不移动 |
| D、恒温恒容,平衡前后混合气体的密度保持不变 |
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知H-H键键能为436kJ?mol-1,N-H键键能为391kJ?mol-1,根据热化学方程式:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.则N≡N键的键能( 单位:kJ?mol-1 )是( )
| A、431 | B、649 |
| C、896 | D、945.6 |
对于相同体积的K2CO3溶液(浓度为c1)和(NH4)2CO3溶液(浓度为c2),若其中CO32-的物质的量浓度相同,则c1和c2的关系是( )
| A、c1=c2 |
| B、c1>c2 |
| C、c1≥c2 |
| D、c1<c2 |
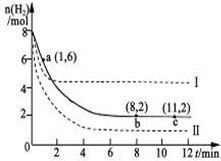 工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )
工业上可用CO2生产甲醇,反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图实线所示.图中虚线表示仅改变某一反应条件时,H2物质的量随时间的变化.下列说法正确的是( )| A、曲线Ⅱ对应的条件改变是降低压强 |
| B、若曲线I对应的条件改变是升高温度,则该反应△H>0 |
| C、反应开始至a点时v(H2)=1mol?L-1?min-1 |
| D、其它条件不变,若降低该反应的温度,平衡常数值将减小 |
 )具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式:
)具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药.写出阿司匹林与足量NaOH溶液共热反应的化学方程式: