题目内容
19.决定元素种类的是( )| A. | 质子数 | B. | 电子数 | C. | 中子数 | D. | 质子数和中子数 |
分析 决定元素种类的是核内质子数或核电荷数.
解答 解:根据不同种元素最本质的区别是质子数(或核电荷数)不同,元素的种类由质子数决定.
故选A.
点评 本题考查原子构成,题目难度不大,解答本题关键是要知道决定元素种类的是核内质子数或核电荷数.

练习册系列答案
相关题目
9.下列事实不能说明醋酸属于弱电解质的是( )
| A. | 0.1mol/L CH3COONa溶液显碱性 | |
| B. | 0.1mol/L醋酸溶液的pH=3 | |
| C. | 物质的量浓度相同的盐酸和醋酸同时与锌反应,开始时锌粒跟盐酸反应比跟醋酸反应的速率快 | |
| D. | 中和100mL1mol/L 的CH3COOH溶液需要100mL1mol/L的NaOH溶液 |
10.下列各项叙述中,正确的是( )
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 第一电离能由小到大的顺序是S<P<Cl | |
| C. | 47Ag原子的价层电子排布式是4d95s2 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是p区元素 |
7.二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如图1:
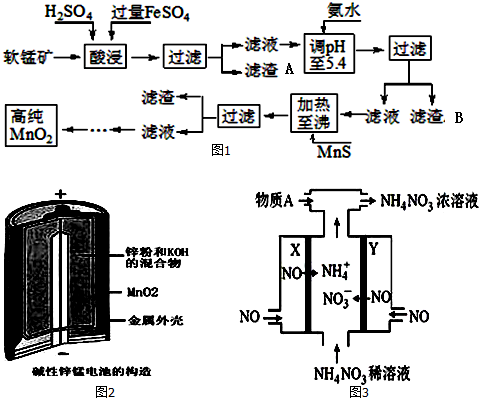
某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为MnO2+2FeSO4+2H2SO4═MnSO4+Fe2(SO4)3+2H2O.
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(2)滤渣A的主要成分是SiO2;滤渣B的主要成分是Fe(OH)3、Al(OH)3.
(3)加入MnS的目的是除去Cu2+、Zn2+杂质.可能原因是CuS、ZnS的溶解度较MnS小.
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为MnO2+H2O+e-═MnO(OH)+OH-,电池总反应的方程式为Zn+2MnO2+2H2O═2MnOOH+ZnOH)2.
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极阴极,电解时阳极的电极反应为NO-3e-+2H2O=NO3-+4H+,使电解产物全部转化为NH4NO3,需补充物质A,A是NH3.
14.下列各组溶液,不用其它试剂就不能将它们区别开的是( )
| A. | 石灰水和碳酸钠 | B. | 偏铝酸钠和盐酸 | ||
| C. | 石灰水和磷酸 | D. | 硫酸铝和氢氧化钠 |
4.已知:S(s)+O2(g)→SO2(g)+297.16kJ,2SO2(g)+O2(g)═2SO3(g)+196.6kJ,下列说法正确的是( )
| A. | 1molSO2(g)的能量总和大于lmolS(s)和lmolO2(g)的能量总和 | |
| B. | 将2molSO2(g)与lmolO2(g)在一定条件下充分反应,放出196.6kJ的热量 | |
| C. | S(g)+O2(g)→SO2(g)+Q,Q值小于297.16kJ | |
| D. | 当lmolS(s)完全转化为SO3(g)时(假设无热量损失),放出395.46kJ的热量 |
11.下列溶液中的c(Cl-)与50mL1mol/LFeCl3溶液中的c(Cl-)相等的是( )
| A. | 1mol/LNaCl溶液 | B. | 2mol/LNH4Cl溶液 | ||
| C. | 1.5mol/LMgCl2溶液 | D. | 2mol/LAlCl3溶液 |
8.关于化学平衡常数的叙述正确的是( )
| A. | 温度一定,一个化学反应的平衡常数是一个常数 | |
| B. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| C. | 温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数 | |
| D. | 浓度商Qc<Kc,v(正)<v(逆) |
9.某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中舍有Ni70.0%及一定量的Al、Fe、SiO2和有机物,镍及其化台物的化学性质与铁的类似,但Ni2-的性质较稳定).
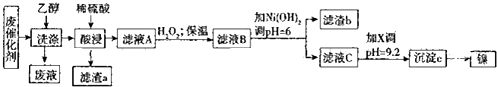
已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
(1)滤渣a的成分是SiO2,用乙醇洗涤废催化剂的目的是溶解、除去有机物,从废渣中回收乙醇的方法是蒸馏.
(2)为提高酸浸速率,可采取的措施有(答两条)将废催化剂粉碎或适当地提高硫酸的浓度、浸泡时的温度.
(3)向A中加人 H2O2时反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.试剂x可以是蒸馏.
(4)用方程式表示出由沉淀.制取单质镍的方法Ni(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$NiO+H2O、2Al+2NiO $\frac{\underline{\;高温\;}}{\;}$Al2O3+3Ni.回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了akgNi(OH)2,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为(70%×97%m+$\frac{59}{93}$a)×95%kg(填计算式).
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应.与电镀相比,化掌镀的最大优点是:不消耗电能,节约能源.

已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(2)为提高酸浸速率,可采取的措施有(答两条)将废催化剂粉碎或适当地提高硫酸的浓度、浸泡时的温度.
(3)向A中加人 H2O2时反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.试剂x可以是蒸馏.
(4)用方程式表示出由沉淀.制取单质镍的方法Ni(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$NiO+H2O、2Al+2NiO $\frac{\underline{\;高温\;}}{\;}$Al2O3+3Ni.回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了akgNi(OH)2,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为(70%×97%m+$\frac{59}{93}$a)×95%kg(填计算式).
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应.与电镀相比,化掌镀的最大优点是:不消耗电能,节约能源.