题目内容
10.在实验室里可按图所示的装置来干燥收集气体R,多余的气体可用水来吸收,则R是( )
| A. | Cl2 | B. | SO2 | C. | NO2 | D. | NH3 |
分析 该装置的收集装置是利用向下排空气法收集,则收集的气体密度小于空气密度,且和氧气不反应,尾气处理装置中用水吸收气体,且使用防倒吸装置,说明该气体极易溶于水,并注意酸性气体不能碱石灰、氨气不能用无水氯化钙来干燥,以此解答该题.
解答 解:A.Cl2的密度大于空气的密度,采用多用瓶收集时应长进短出,故A错误;
B.SO2尾气须用碱性溶液吸收,SO2密度大于空气的密度,采用集气瓶收集时应长进短出,不符合图中装置要求,故B错误;
C.二氧化氮和水反应生成一氧化氮气体,不能用水吸收,且不能用向下排空法收集,故C错误;
D.氨气密度小于空气密度,且极易溶于水,能够用固体碱石灰干燥,故D正确.
故选D.
点评 本题考查实验装置的选择,解答本题时既要考虑物质的水溶性,又要考虑气体是否能和干燥剂发生化学反应,完成此题,可以依据物质的性质进行,题目难度不大.

练习册系列答案
相关题目
20.下列数字为几种元素的原子序数,其中位于周期表第三周期的是( )
| A. | 1 | B. | 7 | C. | 8 | D. | 12 |
18.下列说法不正确的是( )
| A. | 实验室制乙烯时不能将产生的气体直接通入酸性高锰酸钾溶液中来检验乙烯,应先通过足量氢氧化钠溶液吸收挥发出来的乙醇并除去二氧化硫 | |
| B. | 实验室制乙炔时不能将产生的气体直接通入酸性高锰酸钾溶液中来检验乙炔,应先通过足量的硫酸铜溶液除去硫化氢等杂质 | |
| C. | 探究乙酸乙酯在不同浓度碱溶液条件下水解速率可以通过其他条件相同时酯层完全消失的时间来判断 | |
| D. | 乙醇可以被足量酸性高锰酸钾溶液氧化为乙酸,故甲醇可以被足量酸性高锰酸钾溶液氧化为甲酸 |
5.如图形象地表示了氯化钠的形成过程.下列相关叙述中不正确的是( )


| A. | 钠原子易失去一个电子,氯原子易得到一个电子 | |
| B. | 钠离子与钠原子有相似的化学性质 | |
| C. | 钠原子与氯原子作用生成NaCl后,其稳定性增强 | |
| D. | 氯化钠是离子化合物 |
2.两份等质量的铝粉,一份加入足量氢氧化钠溶液中,一份加入足量盐酸中,充分反应后收集到相同条件下的氢气体积比为( )
| A. | 1:1 | B. | 2:1 | C. | 1:4 | D. | 1:2 |
19.NA为阿伏加德罗常数,下述正确的是( )
| A. | 64gSO2含有硫原子数为2NA | |
| B. | NA个氧分子和NA个氢分子的质量比等于16:1 | |
| C. | 常温常压下,11.2L氧气所含的原子数为NA | |
| D. | 标准状况下,22.4L的水含有NA个水分子 |
20.工业上通过2Al2O3+3C+6Cl2$\frac{\underline{\;高温\;}}{\;}$4AlCl3+3CO2制取无水氯化铝,下列说法正确的是( )
| A. | Cl2发生氧化反应 | B. | Cl2是还原剂 | ||
| C. | 若生成11gCO2,则转移3mol电子 | D. | C失去电子 |
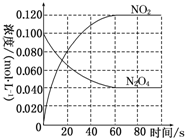 在容积为1.00L的容器中,通入一定量的N2O4(g),发生反应,随温度升高,混合气体的颜色变深.
在容积为1.00L的容器中,通入一定量的N2O4(g),发生反应,随温度升高,混合气体的颜色变深.