题目内容
高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)?Fe(s)+CO2(g)△H>0.已知1100℃时,K=0.26
(1)写出该反应的平衡常数表达式: .
(2)温度升高,化学平衡移动后达到新的平衡,平衡常数K值 (填“增大”、“减小”或“不变”).
(3)1100℃时,测得高炉中c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,在这种情况下,该反应 (填“已”或“没有”)处于化学平衡状态,此时化学反应速率V正 V逆.(填“大于”、“小于”或“等于”).
(1)写出该反应的平衡常数表达式:
(2)温度升高,化学平衡移动后达到新的平衡,平衡常数K值
(3)1100℃时,测得高炉中c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,在这种情况下,该反应
考点:用化学平衡常数进行计算,化学平衡常数的含义
专题:
分析:(1)依据平衡常数的概念书写;
(2)升高温度平衡向吸热方向移动,根据平衡移动的方向判断平衡常数K值;
(3)依据浓度计算浓度商结合平衡常数进行比较判断反应进行的方向.
(2)升高温度平衡向吸热方向移动,根据平衡移动的方向判断平衡常数K值;
(3)依据浓度计算浓度商结合平衡常数进行比较判断反应进行的方向.
解答:
解:(1)固体不在平衡表达式中出现,平衡常数表达式K=
,故答案为:
;
(2)反应吸热,升高温度平衡向正反应方向移动,平衡常数K值增大,故答案为:增大;
(3)1100℃时测得高炉中c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,浓度商Q=
=0.25<K=0.26,说明平衡正向进行,反应未达到平衡,v正>v逆,
故答案为:没有;大于.
| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
(2)反应吸热,升高温度平衡向正反应方向移动,平衡常数K值增大,故答案为:增大;
(3)1100℃时测得高炉中c(CO2)=0.025mol?L-1,c(CO)=0.1mol?L-1,浓度商Q=
| 0.025mol/L |
| 0.1mol/L |
故答案为:没有;大于.
点评:本题主要考查了化学平衡移动、平衡常数、化学平衡状态,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
合金是一类用途广泛的金属材料.下列物质中,属于合金的是( )
| A、铁 | B、铝 | C、钢 | D、钠 |
今年世界地球日主题为“珍惜地球资源 转变发展方式”.下列做法违背该主题的是( )
| A、利用秸杆、垃圾发电 |
| B、利用太阳能、地热能等清洁能源 |
| C、回收利用废旧金属 |
| D、大量开采、使用化石燃料 |
下列关于胶体的说法正确的( )
| A、胶体与溶液的分离可采用过滤的方法 |
| B、胶体与溶液的本质区别是有丁达尔效应 |
| C、将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D、胶体属于介稳体系 |
以下各常数随着温度的升高不一定增大的是( )
| A、Kw | B、K | C、Ka | D、Kb |
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、2CN-+H2O+CO2→2HCN+CO32- |
| B、2HCOOH+CO32-→2HCOO-+H2O+CO2↑ |
| C、中和等体积、等c(H+)的HCOOH和HCN消耗NaOH的量前者小于后者 |
| D、相同物质量浓度的HCOONa和NaCN溶液中:c(HCOO-)<c(CN-) |
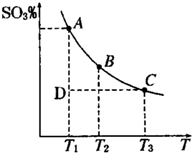 运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义.