题目内容
(17分)电化学原理在日常生活和工农业生产中发挥着重要作用。钢铁生锈现象随处可见,钢铁的电化腐蚀原理如图所示:

(1)写出石墨电极的电极反应_________________________;
(2)将该装置作简单修改即可成为钢铁电化学防护的装置,请在上图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向且完成以下问题
①简单修改后的该防护装置的名称为__________________________________
写出修改后石墨电极的电极反应式____________________________________;
②_______极(填“正极”“负极”“阳极”“阴极”)附近溶液的pH增大;
③检验阳极产物的方法是_____________________________________________;
④修改后的装置共收集到标准状况下的气体11.2 L时,则有______mol电子发生转移,假设溶液的体积为200ml,则此时溶液中OH-的物质的量浓度为________ mol/L
(1)O2+2H2O+4e-===4OH-(2)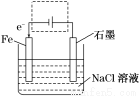 ;①外加电流的阴极保护法;2Cl- -2e-=Cl2↑;②阴极;③用湿润的淀粉KI试纸靠近阳极,如果试纸变蓝,说明是Cl2;④ 0.52.5
;①外加电流的阴极保护法;2Cl- -2e-=Cl2↑;②阴极;③用湿润的淀粉KI试纸靠近阳极,如果试纸变蓝,说明是Cl2;④ 0.52.5
【解析】
试题分析:(1)中性条件下,钢铁发生吸氧腐蚀,铁作负极,石墨作正极,正极上氧气得电子生成氢氧根离子,所以电极反应式为:O2+4e-+2H2O=4OH-,故答案为:O2+4e-+2H2O=4OH-;(2)①要保护钢铁不受腐蚀,可以把铁设计成电解池的阴极,与电源负极相连接,名称为外加电源的阴极保护法;②阴极上氢离子得电子生成氢气,故阴极显碱性,PH增大;③电解质溶液为氯化钠溶液,石墨电极上有氯气生成,检验氯气的方法为用湿润的淀粉KI试纸靠近阳极,如果试纸变蓝,说明是Cl2 ;④11.2L气体的物质的量为0.5mol,生成氢气和氯气的总物质的量为0.5mol,生成氢气和氯气的物质的量分别为0.25mol,每生成1mol氢气转移2mol电子,故转移电子的物质的量为0.25molx2=0.5mol;转移电子数与阴极生成氢氧根离子的物质的量相等,故氢氧根离子的物质的量为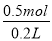 =2.5mol/L.,答案为:
=2.5mol/L.,答案为: ①外加电流的阴极保护法;2Cl- -2e-=Cl2↑;②阴极;③用湿润的淀粉KI试纸靠近阳极,如果试纸变蓝,说明是Cl2 ④ 0.5 2.5
①外加电流的阴极保护法;2Cl- -2e-=Cl2↑;②阴极;③用湿润的淀粉KI试纸靠近阳极,如果试纸变蓝,说明是Cl2 ④ 0.5 2.5
考点:原电池和电解池

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案 2SO3(g)△H=-Q kJ?mol-1 (Q>0),则将 2NA 个SO2分子和 NA 个O2分子置于一密闭容器中充分反应后放出QkJ的热量
2SO3(g)△H=-Q kJ?mol-1 (Q>0),则将 2NA 个SO2分子和 NA 个O2分子置于一密闭容器中充分反应后放出QkJ的热量
 2PbSO4 + 2H2O根据此反应判断下列叙述中正确的是
2PbSO4 + 2H2O根据此反应判断下列叙述中正确的是
 +□ =□MnO2↓+□Cl2↑+□
+□ =□MnO2↓+□Cl2↑+□