题目内容
5.某兴趣小组用如图装置做了两次实验,不可思议地用原电池完成总反应:H++OH-=H2O实验①:向甲池的Pt电极表面通氢气,发现电流计指针发生了偏转,乙池的Pt电极表面出现气泡.
实验②:向乙池的Pt电极表面通入另一气体,发现电流计指针也发生了偏转,且偏转方向与实验①相同,同时甲池的Pt电极表面也出现气泡.
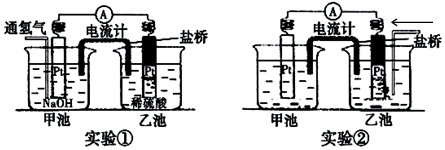
(1)实验①,甲池通氢气的Pt电极为负极,电极反应式为2H2-4e-+4OH-=2H2O.
(2)实验②中乙池中通入气体为O2,甲池电解质溶液为NaOH.
分析 (1)燃烧电池中通入氢气的一极为负极,碱性条件下,氢气失电子生成水;
(2)实验②中乙池中通入气体,形成原电池,且电流计指针偏转方向与实验①相同,所以乙池为正极.
解答 解:(1)燃烧电池中通入氢气的一极为负极,碱性条件下,氢气失电子生成水,则负极的电极反应方程式为:2H2-4e-+4OH-=2H2O;
故答案为:负;2H2-4e-+4OH-=2H2O;
(2)实验②中乙池中通入气体,形成原电池,且电流计指针偏转方向与实验①相同,所以乙池为正极,正极上氧气得电子,即实验②中乙池中通入气体为O2;甲池中电解质为NaOH;
故答案为:O2;NaOH.
点评 本题考查了原电池的原理,明确各个电极上发生的反应是解本题关键,注意把握电解质溶液对电极反应的影响,题目难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
15.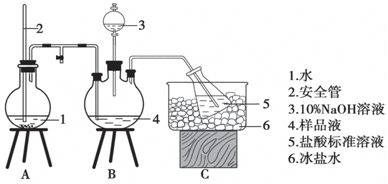 某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.
某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL c1 mol•L-1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用c2 mol•L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液.
②氯的测定
回答下列问题:
(1)装置中安全管的作用原理是使A瓶中压强稳定.
(2)用NaOH标准溶液滴定过剩的HCl时,应使用碱式滴定管,可使用的指示剂为酚酞或甲基橙.
(3)样品中氨的质量分数表达式为$\frac{(C{\;}_{1}V{\;}_{1}-C{\;}_{2}V{\;}_{2})×10{\;}^{-3}×17}{w}$×100%.
(4)测定氨前应该对装置进行气密性检查,若气密性不好测定结果将偏低(填“偏高”或“偏低”).
(5)氯的测定采用莫尔法,莫尔法是一种沉淀滴定法,用标准硝酸银溶液滴定,进行测定溶液中Cl-的浓度.已知:
①若用AgNO3溶液滴定待测液,可选为滴定指示剂的是C.
A.NaCl B.BaBr2 C.Na2CrO4 D.KSCN
②滴定终点的现象是滴入最后一滴标准溶液,生成砖红色沉淀,且30s 不复原.
 某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.
某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL c1 mol•L-1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用c2 mol•L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液.
②氯的测定
回答下列问题:
(1)装置中安全管的作用原理是使A瓶中压强稳定.
(2)用NaOH标准溶液滴定过剩的HCl时,应使用碱式滴定管,可使用的指示剂为酚酞或甲基橙.
(3)样品中氨的质量分数表达式为$\frac{(C{\;}_{1}V{\;}_{1}-C{\;}_{2}V{\;}_{2})×10{\;}^{-3}×17}{w}$×100%.
(4)测定氨前应该对装置进行气密性检查,若气密性不好测定结果将偏低(填“偏高”或“偏低”).
(5)氯的测定采用莫尔法,莫尔法是一种沉淀滴定法,用标准硝酸银溶液滴定,进行测定溶液中Cl-的浓度.已知:
| 银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| 溶解度(mol•L-1) | 1.3410-6 | 7.110-7 | 1.110-8 | 6.510-5 | 1.010-6 |
A.NaCl B.BaBr2 C.Na2CrO4 D.KSCN
②滴定终点的现象是滴入最后一滴标准溶液,生成砖红色沉淀,且30s 不复原.
14.下列离子方程式,正确的是( )
| A. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ | |
| B. | 氧化铁与稀盐酸反应:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 锌与硝酸银溶液反应:Zn+Ag+═Zn2++Ag | |
| D. | 在硫酸溶液中加入氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
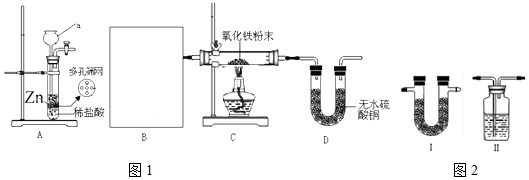
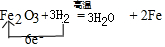 .实验结束时应该采取的操作是先停止加热,冷却到室温,再停止通H2.
.实验结束时应该采取的操作是先停止加热,冷却到室温,再停止通H2.