题目内容
 A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增.已知B、D两种元素原子的最外层电子数是最内层电子数的两倍,而C元素原子的最外层电子数等于B元素原子的核外电子数,E的价电子数为1.回答下列问题.
A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增.已知B、D两种元素原子的最外层电子数是最内层电子数的两倍,而C元素原子的最外层电子数等于B元素原子的核外电子数,E的价电子数为1.回答下列问题.(1)画出C元素的原子结构示意图
(2)在1mol DC2中,有
(3)在化合物BC2的晶体中,每个BC2分子周围与它距离最近的BC2分子有
(4)原子序数介于B、C之间的元素X和B、C都可与A形成10e-的化合物.则X、B、C的第一电离能顺序是
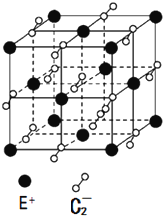
(5)已知高温下C和E元素形成的晶体呈立方体结构,晶体中元素C的化合价部分为0价,部分为-2价.如图所示为C和E元素形成的晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是
A.该晶体化学式为EC2(KO2),每个晶胞含有个4个E+和4个C2-
B.晶体中每个E+周围有8个C2-,每个C2-周围有8个E+
C.晶体中与每个E+距离最近的E+有8个
D.晶体中,0价C与-2价C的数目比为3:1
E.C2-与N2互为等电子体.
考点:位置结构性质的相互关系应用,晶胞的计算
专题:
分析:A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增.B、D两种元素原子的最外层电子数是最内层电子数的两倍,最外层电子数为4,处于ⅣA族,则B为碳元素、D为Si;C元素原子的最外层电子数等于B元素原子的核外电子数,C原子最外层电子数为6,处于ⅥA族,原子序数小于Si,则C为O元素;E的价电子数为1,原子序数大于Si,则E为K元素;(4)中X原子序数介于B、C之间,则X为N元素,元素X和B、C都可与A形成10e-的化合物,则A为H元素,据此解答.
解答:
解:A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增.B、D两种元素原子的最外层电子数是最内层电子数的两倍,最外层电子数为4,处于ⅣA族,则B为碳元素、D为Si;C元素原子的最外层电子数等于B元素原子的核外电子数,C原子最外层电子数为6,处于ⅥA族,原子序数小于Si,则C为O元素;E的价电子数为1,原子序数大于Si,则E为K元素,
(1)C为O元素,原子结构示意图为: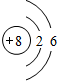 ,故答案为:
,故答案为: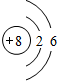 ;
;
(2)SiO2属于原子晶体,每个Si原子形成4个Si-O键,1mol SiO2中有4mol Si-O键,故答案为:4;
(3)CO2晶体中分子之间只有范德华力,为分子密堆积,晶胞为面心立方结构,二氧化碳分子位于顶点与面心,以顶点CO2分子研究,与之距离最近的CO2分子位于面心,每个顶点为12个面共用,故每个CO2分子周围与它距离最近的CO2有12个,故答案为:12;
(4)X原子序数介于B、C之间,则X为N元素,元素X和B、C都可与A形成10e-的化合物,则A为H元素,同周期随原子序数增大,第一电离能呈增大趋势,氮元素2p轨道容纳3个电子,为半满稳定状态,能量较低,第一电离能高于氧元素,故第一电离能N>O>C,三种10e-的化合物为CH4、NH3、H2O,常温下,水为液态,甲烷与氨气为气态,水的沸点最高,氨气分子之间存在氢键,其沸点比甲烷高,故沸点最低的是CH4,故答案为:N>O>C;CH4;
(5)高温下O和K元素形成的晶体呈立方体结构,晶体中元素O的化合价部分为0价,部分为-2价,
A、由晶胞图可知,K+的个数为8×
+6×
=4,O2-的个数为12×
+1=4,化学式为KO2,故A正确;
B、由晶胞图可知,晶体中每个K+周围有6个O2-,每个O2-周围有6个K+,故B错误;
C、由晶胞图可知,以顶点K+研究,与之距离最近的K+位于面心,每个顶点为12个面共用,故每个K+周围与它距离最近的K+有12个,故C错误;
D、晶胞中K+与O2-个数分别为4、4,所以晶胞中共有8个氧原子,根据电荷守恒-2价O原子数目为2,所以0价氧原子数目为8-2=6,所以晶体中,0价氧原子与-2价氧原子的数目比为3:1,故D正确;
E.O2-与N2的原子数目相等,但电子总数或价电子总数不相等,二者不是等电子体,故E错误,
故答案为:AD.
(1)C为O元素,原子结构示意图为:
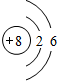 ,故答案为:
,故答案为: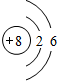 ;
;(2)SiO2属于原子晶体,每个Si原子形成4个Si-O键,1mol SiO2中有4mol Si-O键,故答案为:4;
(3)CO2晶体中分子之间只有范德华力,为分子密堆积,晶胞为面心立方结构,二氧化碳分子位于顶点与面心,以顶点CO2分子研究,与之距离最近的CO2分子位于面心,每个顶点为12个面共用,故每个CO2分子周围与它距离最近的CO2有12个,故答案为:12;
(4)X原子序数介于B、C之间,则X为N元素,元素X和B、C都可与A形成10e-的化合物,则A为H元素,同周期随原子序数增大,第一电离能呈增大趋势,氮元素2p轨道容纳3个电子,为半满稳定状态,能量较低,第一电离能高于氧元素,故第一电离能N>O>C,三种10e-的化合物为CH4、NH3、H2O,常温下,水为液态,甲烷与氨气为气态,水的沸点最高,氨气分子之间存在氢键,其沸点比甲烷高,故沸点最低的是CH4,故答案为:N>O>C;CH4;
(5)高温下O和K元素形成的晶体呈立方体结构,晶体中元素O的化合价部分为0价,部分为-2价,
A、由晶胞图可知,K+的个数为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
B、由晶胞图可知,晶体中每个K+周围有6个O2-,每个O2-周围有6个K+,故B错误;
C、由晶胞图可知,以顶点K+研究,与之距离最近的K+位于面心,每个顶点为12个面共用,故每个K+周围与它距离最近的K+有12个,故C错误;
D、晶胞中K+与O2-个数分别为4、4,所以晶胞中共有8个氧原子,根据电荷守恒-2价O原子数目为2,所以0价氧原子数目为8-2=6,所以晶体中,0价氧原子与-2价氧原子的数目比为3:1,故D正确;
E.O2-与N2的原子数目相等,但电子总数或价电子总数不相等,二者不是等电子体,故E错误,
故答案为:AD.
点评:本题是对物质结构的考查,涉及核外电子排布、电离能、晶体结构与计算等,侧重考查晶胞问题,需要学生具有一定观察与空间想象能力,掌握晶胞中利用均摊法的有关计算,(2)(3)为易错点,注意识记中学常见晶胞结构,难度中等.

练习册系列答案
相关题目
下列关于化学平衡状态的说法中正确的是( )
| A、改变外界条件不能改变化学平衡状态 |
| B、当某反应在一定条件下反应物转化率保持不变时即达到了化学平衡状态 |
| C、当某反应体系中气体的压强不再改变时,该反应一定达到平衡状态 |
| D、当某反应达到平衡状态时,反应物和生成物的浓度一定相等 |
下列实验操作中,正确的是( )
| A、为使过滤速率加快,可用玻璃棒在过滤器中轻轻搅拌,加速液体流动 |
| B、用酒精灯给试管加热时,要将被加热的试管放在酒精灯火焰的外焰上 |
| C、为加速固体物质的溶解只能采用加热的方法 |
| D、为增大气体物质的溶解度,常采取搅拌、加热等措施 |
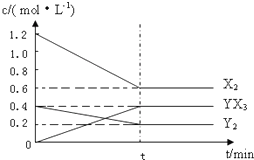 已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素.
已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X2Z,X2Z2两种化合物,W是短周期主族元素中半径最大的元素.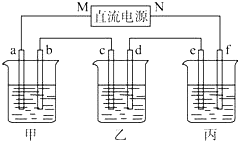 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放NaCl溶液、足量的AgNO3溶液和 K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放NaCl溶液、足量的AgNO3溶液和 K2SO4溶液,电极均为石墨电极.