题目内容
下列物质是弱电解质的是( )
| A、CO2 |
| B、NaCl |
| C、Br2 |
| D、H2O |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:弱电解质是在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐.
解答:
解:A、二氧化碳为非电解质,因此不是弱电解质,故A错误;
B、NaCl在水溶液中完全电离,是强电解质,故B错误;
C、溴单质既不属于电解质也不属于非电解质,因此不是弱电解质,故C错误;
D、水电离程度很小,属于弱电解质,故D正确;
故选D.
B、NaCl在水溶液中完全电离,是强电解质,故B错误;
C、溴单质既不属于电解质也不属于非电解质,因此不是弱电解质,故C错误;
D、水电离程度很小,属于弱电解质,故D正确;
故选D.
点评:本题考查了强弱电解质的判断,难度不大,明确:电解质的强弱是以电离程度判断的,不是以导电能力大小判断的.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质的主要成分正确的是( )
| A、赤铁矿:Fe3O4 |
| B、小苏打:NaHCO3 |
| C、磁铁矿:Fe2O3 |
| D、明矾:KAl(SO4)2 |
下列化学方程式中,不能用离子方程式Ba2++SO42-═BaSO4 表示的是( )
| A、BaCl2+K2SO4═BaSO4+2 KCl |
| B、Ba(OH)2+K2SO4═BaSO4+2 KOH |
| C、Ba(NO3)2+H2SO4═BaSO4+2 HNO3 |
| D、Ba(OH)2+H2SO4═BaSO4+2 H2O |
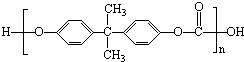 2010年5月1日上海世博会隆重开幕,世博会的环保概念是人们关心的话题,环保材料更为世人瞩目,其中聚碳酸酯是用得较多的材料.聚碳酸酯的结构简式如图所示,下列说法正确的是( )
2010年5月1日上海世博会隆重开幕,世博会的环保概念是人们关心的话题,环保材料更为世人瞩目,其中聚碳酸酯是用得较多的材料.聚碳酸酯的结构简式如图所示,下列说法正确的是( )| A、它在结构上可以看成由碳酸和另一有机物通过缩聚反应而成 |
| B、该有机物是一种高分子化合物,肯定易溶于水 |
| C、它是一种纯净物,属于酯类物质 |
| D、它耐强酸,强碱,不可与强氧化剂发生反应 |
有关化学用语正确的是( )
| A、苯的结构简式C6H6 |
| B、乙烯的结构简式CH2CH2 |
C、四氯化碳的电子式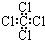 |
| D、乙酸的分子式C2H4O2 |
下列实验装置、试剂选用或操作正确的是( )
A、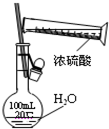 配制一定浓度的稀硫酸 |
B、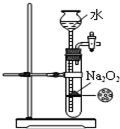 实验室制备氧气 |
C、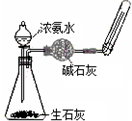 实验室制备氨气 |
D、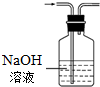 除去CO2中的HCl |
下列物质中含有非极性键且为盐的是( )
| A、CH3COONa |
| B、NH4Cl |
| C、CaCl2 |
| D、H2O2 |
X、Y、Z、W是前20号元素中的4种元素,分布在三个周期,原子序数依次增大,它们可以组成某矿物质:WYZX,四种元素中W,Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y,Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z单质是一种良好的半导体.下列说法不正确的是( )
| A、原子半径:W>Y>Z>X |
| B、气态氢化物的稳定性:X>Z |
| C、金属性:Y<W |
| D、Y、Z的氧化物都能和酸或碱反应,都是两性氧化物 |
已知下列热化学方程式:
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
Fe2O3(s)+
CO(g)═
Fe3O4(s)+
CO2(g)△H=-15.73kJ/mol
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol
则28g CO气体还原足量FeO固体得到Fe单质和CO2气体时对应的△H约为( )
Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-24.8kJ/mol
Fe2O3(s)+
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 3 |
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol
则28g CO气体还原足量FeO固体得到Fe单质和CO2气体时对应的△H约为( )
| A、-218kJ/mol |
| B、-436kJ/mol |
| C、+218kJ/mol |
| D、+436kJ/mol |