题目内容
某厂以工业粗盐(含Ca2+、Mg2+、SO42-等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如图所示:
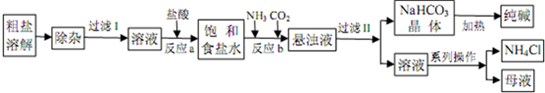
请回答下列问题:
(1)“除杂”步骤中需加入两种试剂,按加入顺序写出其名称 ;
(2)反应“b”的化学反应方程式 ;
(3)“过滤II”所得“溶液”中除NH4+和Cl-外,阴离子有 ;对该溶液的系列操作包括 、 、过滤.
(4)工业纯碱的等级标准如图所示:
取10.00g某纯碱样品配成200mL溶液,取50.00mL溶液加入过量的CaCl2溶液,充分反应后过滤,洗涤沉淀、干燥,称得沉淀质量为2.34g,请经过计算判断该纯碱样品的等级,并求出所配溶液中Na2CO3的物质的量浓度.

请回答下列问题:
(1)“除杂”步骤中需加入两种试剂,按加入顺序写出其名称
(2)反应“b”的化学反应方程式
(3)“过滤II”所得“溶液”中除NH4+和Cl-外,阴离子有
(4)工业纯碱的等级标准如图所示:
| 等级 | 优等品 | 一等品 | 合格品 |
| Na2CO3含量 | ≥99.2 | ≥98.8 | ≥98.0 |
考点:纯碱工业(侯氏制碱法)
专题:元素及其化合物,化学应用
分析:(1)碳酸钠可以将钙离子以及过量的钡离子沉淀下来;除镁离子用氢氧化钠,除钙离子用碳酸钠,除硫酸根离子用氯化钡,所加试剂要过量,为了将多余的杂质除掉,碳酸钠必须放在氯化钡的后面;
(2)将NH3和CO2通入饱和食盐水中,生成NaHCO3和NH4Cl;
(3)向饱和食盐水中通入NH3和CO2后,所得悬浊液中含NaHCO3、NH4Cl和NaCl,据此分析经过滤II后所得溶液的成分;由溶液要得NH4Cl,需经蒸发浓缩、冷却结晶和过滤等操作.
(4)设出50mL纯碱溶液中Na2CO3的物质的量,然后根据所得沉淀的量求出碳酸钠的物质的量,并利用C=
和ω=
×100%来计算.
(2)将NH3和CO2通入饱和食盐水中,生成NaHCO3和NH4Cl;
(3)向饱和食盐水中通入NH3和CO2后,所得悬浊液中含NaHCO3、NH4Cl和NaCl,据此分析经过滤II后所得溶液的成分;由溶液要得NH4Cl,需经蒸发浓缩、冷却结晶和过滤等操作.
(4)设出50mL纯碱溶液中Na2CO3的物质的量,然后根据所得沉淀的量求出碳酸钠的物质的量,并利用C=
| n |
| V |
| m(碳酸钠) |
| m(样品) |
解答:
解:(1)除Mg2+用OH-,除SO42-用Ba2+,除Ca2+用CO32-,故除去Ca2+、Mg2+、SO42-等杂质离子,所加的两种试剂为:氢氧化钡、碳酸钠溶液;加试剂要过量,Na2CO3可以将Ca2+以及过量的Ba2+沉淀下来,为了将多余的杂质除掉,碳酸钠必须放在氯化钡的后面;故答案为:氢氧化钡、碳酸钠溶液;
(2)将NH3和CO2通入饱和食盐水中,生成NaHCO3和NH4Cl,NaHCO3的溶解度较小,以晶体的形式析出,化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(3)向饱和食盐水中通入NH3和CO2后,所得悬浊液中含NaHCO3、NH4Cl和NaCl,经过滤II将大部分的NaHCO3过滤得NaHCO3晶体,所得溶液中的成分有NaHCO3、NH4Cl和NaCl,故溶液中除NH4+和Cl-外,阴离子有HCO3-;由溶液要得NH4Cl,需经蒸发浓缩、冷却结晶和过滤等操作,故答案为:HCO3-;蒸发浓缩、冷却结晶;
(4)设50mL纯碱溶液中Na2CO3的物质的量为 xmol,由于沉淀CaCO3质量为2.34g,则CaCO3的物质的量n=
=0.0234mol,
Na2CO3 ~CaCO3
1 1
x 0.0234mol
则有:
=
,
解得x=0.0234mol
则c(Na2CO3)=
=0.468mol?L-1,
ω(Na2CO3)=
=0.99216>0.992,为优等品.
答:该纯碱样品的等级为优等品,所配溶液中Na2CO3的物质的量浓度为0.468mol/L.
(2)将NH3和CO2通入饱和食盐水中,生成NaHCO3和NH4Cl,NaHCO3的溶解度较小,以晶体的形式析出,化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(3)向饱和食盐水中通入NH3和CO2后,所得悬浊液中含NaHCO3、NH4Cl和NaCl,经过滤II将大部分的NaHCO3过滤得NaHCO3晶体,所得溶液中的成分有NaHCO3、NH4Cl和NaCl,故溶液中除NH4+和Cl-外,阴离子有HCO3-;由溶液要得NH4Cl,需经蒸发浓缩、冷却结晶和过滤等操作,故答案为:HCO3-;蒸发浓缩、冷却结晶;
(4)设50mL纯碱溶液中Na2CO3的物质的量为 xmol,由于沉淀CaCO3质量为2.34g,则CaCO3的物质的量n=
| 2.34 |
| 100 |
Na2CO3 ~CaCO3
1 1
x 0.0234mol
则有:
| 1 |
| X |
| 1 |
| 0.0234mol |
解得x=0.0234mol
则c(Na2CO3)=
| 0.0234mol |
| 0.05L |
ω(Na2CO3)=
0.0234×
| ||
| 10 |
答:该纯碱样品的等级为优等品,所配溶液中Na2CO3的物质的量浓度为0.468mol/L.
点评:本题考查了 工业制纯碱的原理分析,生产过程中的物质变化,混合物成分的分析判断和计算应用,实验过程分析,题目难度中等.

练习册系列答案
 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
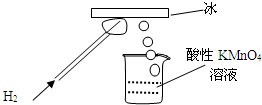 某研究性学习小组做了一个如图所示的实验,在导管口点燃氢气后,发现烧杯中酸性溶液褪色,若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.下列判断正确的是
某研究性学习小组做了一个如图所示的实验,在导管口点燃氢气后,发现烧杯中酸性溶液褪色,若将烧杯中的溶液换成含有少量KSCN的FeCl2溶液,溶液显红色.下列判断正确的是( )
| A、该条件下H2燃烧放出的热量使冰分解产生了氧气 |
| B、该条件下H2被冷却为液态氢,液氢的水溶液具有氧化性 |
| C、该条件下生成的物质具有氧化性和还原性 |
| D、该条件下生成的水分子化学性质比较活泼 |
如图为周期表前四周期的一部分,关于X、Y、Z、M的说法正确的是( )
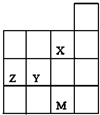

| A、Y、Z的最高价氧化物的水化物酸性为Y<Z |
| B、M的最外层电子数比Z大10 |
| C、X、M的气态氢化物的稳定性M>X |
| D、X、Y形成简单离子的最外层电子均满足8e-稳定结构 |
甲~辛等元素在周期表中的相对位置如图.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )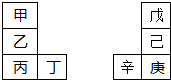

| A、金属性:甲>乙>丁 |
| B、原子半径:辛>己>戊 |
| C、丙与庚的原子核外电子数相差13 |
| D、乙的单质在空气中燃烧生成只含离子键的化合物 |