题目内容
17.对于反应2SO2(g)+O2(g)═2SO3(g),能增大逆反应速率的措施是( )| A. | 恒容通入一定量的SO2 | B. | 增大体系容积 | ||
| C. | 恒容移去部分SO3 | D. | 降低体系温度 |
分析 增大逆反应速率,可增大生成物浓度,升高温度,增大压强,或加入催化剂等,以此解答该题.
解答 解:A.恒容通入一定量的SO2,反应物浓度增大,正反应速率增大,平衡正向移动,生成物浓度增大,逆反应速率增大,故A正确;
B.增大体系容积,浓度减小,反应速率减小,故B错误;
C.移去部分SO3,浓度减小,反应速率减小,故C错误;
D.降低体系的温度,正逆反应速率都减小,故D错误.
故选A.
点评 本题考查化学反应速率的影响因素,侧重于从浓度的角度考查该题,为高考常见题型,难度不大,注意相关基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.一定温度下,在三个体积均为2.0L的恒容密闭容器中发生如下反应:PCl5(g)═PCl3(g)+Cl2(g)
下列说法正确的是( )
| 编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A. | 平衡常数K:容器Ⅱ>容器Ⅲ | |
| B. | 反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ | |
| C. | 反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 mol/(L•s) | |
| D. | 起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行 |
5.下列有关说法正确的是( )
| A. | 凡含有食品添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 可用米汤检验含碘盐中的碘酸钾(KIO3) | |
| C. | 涤纶、绵纶、棉花、羊毛、蚕丝等都是天然纤维素 | |
| D. | 纤维素属于糖类,不能够直接被消化成为人体的营养物质 |
12.有关AgCl的沉淀溶平衡体系,下列说法正确的是( )
| A. | AgCl的沉淀生成和溶解不断进行,但速率不相等 | |
| B. | AgCl难溶于水,溶液中没有Ag+和Cl- | |
| C. | 升高温度,AgCl的溶解度增大 | |
| D. | 向平衡体系中加入NaCl固体,AgCl的溶解度变小 |
2. 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
 氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )
氮化硼(BN)晶体有多种相结构.六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电.立方相氮化硼是超硬材料,有优异的耐磨性.它们的晶体结构如图所示.关于这两种晶体的说法,正确的是( )| A. | 立方相氮化硼含配位键B→N | |
| B. | 六方相氮化硼层间作用力小,所以质地软,熔点低 | |
| C. | 两种氮化硼中的硼原子都是采用sp2杂化 | |
| D. | 六方相氮化硼晶体其结构与石墨相似却不导电,原因是没有可以自由移动的电子 |
9.若在铜片上镀银时,下列叙述正确的是( )
①将铜片接在电源的正极上
②将银片接在电源的正极上,
③在铜片上发生的反应是:Ag++e-═Ag,
④在银片上发生的反应是:O2↑+2H2O+4e-═4OH-,
⑤需用CuSO4溶液作电解液
⑥需用AgNO3溶液作电解液.
①将铜片接在电源的正极上
②将银片接在电源的正极上,
③在铜片上发生的反应是:Ag++e-═Ag,
④在银片上发生的反应是:O2↑+2H2O+4e-═4OH-,
⑤需用CuSO4溶液作电解液
⑥需用AgNO3溶液作电解液.
| A. | ①③⑥ | B. | ②③⑥ | C. | ①④⑤ | D. | ②③④⑥ |
6.某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,下表是他们撰写的实验报告的一部分.
请帮助该小组同学完成实验报告中的内容.
由实验⑥中看到的所有现象:沾有无水硫酸铜粉末的棉花球变蓝;A烧杯中没有明显现象,B烧杯中有白色沉淀生成.可以得出的结论是Na2CO3的热稳定性比NaHCO3强.
写出所有化学方程式说明得出结论的原因.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,Ca(OH)2+CO2=CaCO3↓+H2O.
| 实验序号 | 实验步骤(内容) | 现象 |
| ① | 在贴有标签a、b的试管中分别加入1.0g Na2CO3固体和NaHCO3固体,观察外观. | / |
| ② | 分别滴入几滴水,振荡,摸试管底部. | 试管a放热现象更明显(填“a”或“b”) |
| ③ | 继续向两试管中分别加入10.0mL水,用力振荡,观察现象. | / |
| ④ | 再分别向两试管中滴加2滴酚酞溶液,观察现象. | 溶液均变红,颜色较深的试管是a(填“a”或“b”). |
| ⑤ | 最后分别向两溶液中滴加足量盐酸. | 红色褪去,均有无色气体产生.经计算生成气体的是a<b(填“>”“<”或“=”) |
| ⑥ | 加热大试管一段时间.(注:棉花球沾有无水硫酸铜粉末)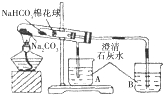 | / |
由实验⑥中看到的所有现象:沾有无水硫酸铜粉末的棉花球变蓝;A烧杯中没有明显现象,B烧杯中有白色沉淀生成.可以得出的结论是Na2CO3的热稳定性比NaHCO3强.
写出所有化学方程式说明得出结论的原因.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,Ca(OH)2+CO2=CaCO3↓+H2O.

 .某油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示:
.某油田开采的石油中溶有一种碳氢化合物--金刚烷,它的分子立体结构如图所示: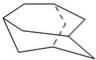
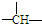 ”结构.
”结构.