题目内容
常温下,0.1mol·L—1某一元酸(HA)溶液中c(OH—)/c(H+)=1×10—8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10—10mol·L—1
B.溶液中c(H+)+c(A—)=0.1mol·L—1
C.与0.05mol·L—1 NaOH溶液等体积混合所得溶液中离子浓度大小关系为:c(A—)> c(Na+)> c(OH—)> c(H+)
D.原溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH—)均增大
D
【解析】
试题分析:溶液中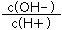 =1×10-8,由Kw=c(H+)×c(OH-)=10-14,可知c(H+)=10-3mol/L,A.溶液中水电离出的c(H+)=c(OH-)=10-11mol/L,错误;B.HA为弱酸不能完全电离,由c(H+)=10-3mol/L可知c(H+)+c(A-)=0.002 mol/L,错误;C.与0.05mol/LNaOH溶液等体积混合后,HA过量,则溶液应呈酸性,应有c(H+)>c(OH-),错误;D.溶液中加入一定量CH3COONa晶体,发生:CH3COO-+H+?CH3COOH,或加入水,都会导致c(H+)减小,c(OH-)增大,正确。
=1×10-8,由Kw=c(H+)×c(OH-)=10-14,可知c(H+)=10-3mol/L,A.溶液中水电离出的c(H+)=c(OH-)=10-11mol/L,错误;B.HA为弱酸不能完全电离,由c(H+)=10-3mol/L可知c(H+)+c(A-)=0.002 mol/L,错误;C.与0.05mol/LNaOH溶液等体积混合后,HA过量,则溶液应呈酸性,应有c(H+)>c(OH-),错误;D.溶液中加入一定量CH3COONa晶体,发生:CH3COO-+H+?CH3COOH,或加入水,都会导致c(H+)减小,c(OH-)增大,正确。
考点:考查弱电解质在水溶液中的电离平衡。

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
常温下,有下列4种溶液,下列说法正确的是
① | ② | ③ | ④ |
0.1 mol·L-1 CH3COOH溶液 | pH=3 CH3COOH溶液 | 0.1 mol ·L-1 NaOH溶液 | pH=11 NaOH溶液 |
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍后,pH与②相同
C.①与③混合,若溶液pH=7,则两种溶液的体积:③>①
D.②与④混合,若溶液pH=7,则两种溶液的体积:④>②
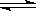 H2+I2
H2+I2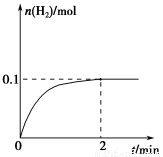
 A+E
A+E