题目内容
7.下列有机物中含有少量杂质(括号中物质是杂质),除杂方法正确的是( )| A. | 乙烯(乙炔):将气体通过盛KMnO4溶液的洗气瓶 | |
| B. | 溴乙烷(溴):加入CCl4,振荡,静置,分液 | |
| C. | 苯(苯酚):加足量NaOH溶液,振荡,静置,分液 | |
| D. | 乙醛(乙酸乙酯):加入NaOH溶液,振荡,静置,分液 |
分析 A.二者均可被高锰酸钾氧化;
B.二者均与溶于四氯化碳;
C.苯酚与NaOH溶液反应后与苯分层;
D.乙酸乙酯与NaOH反应后与乙醛不分层.
解答 解:A.二者均可被高锰酸钾氧化,将原物质反应掉,则不能除杂,故A错误;
B.二者均与溶于四氯化碳,不分层,则不能利用分液分离,故B错误;
C.苯酚与NaOH溶液反应后与苯分层,则振荡,静置,分液可除杂,故C正确;
D.乙酸乙酯与NaOH反应后与乙醛不分层,则不能利用分液分离,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、发生的反应及混合物分离方法等为解答的关键,注意有机物的性质,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
15.下表列出部分化学键的键能:
据此判断下列说法正确的是( )
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C | Cl-Cl |
| 键能/kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 | 243 |
| A. | 表中最稳定的共价键是Si-Si | |
| B. | Cl2(g)→2 Cl(g):△H=-243 kJ•mol | |
| C. | H2 (g)+Cl2(g)=2HCl(g):△H=-183 kJ•mol | |
| D. | 根据表中数据能计算出SiCl4(g)+2 H2(g)=Si(s)+4 HCl(1)的△H |
2.下列烃和H2加成反应可生成3-甲基己烷的是( )
| A. | CH2=CHCH(CH3)CH2CH2CH2CH3 | B. | CH2=CHC(CH3)=CHCH2CH3 | ||
| C. | CH2=CHCH(CH3)C≡CH | D. | CH3CH2CH2CH2C(CH3)=CH2 |
19.风光互补LED照明系统广泛用于高速公路照明,其原理如图所示,图中涉及的能量转化方式有( )


| A. | 至少6种 | B. | 4种 | C. | 3种 | D. | 2种 |
16.在周期表中,下列各组元素位于同主族的是( )
| A. | Mg、Al | B. | Se,Br | C. | Si、Ge | D. | S、As |
17.如表是A、B、C、D、E五种有机物的有关信息;
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学反应方程式 .
.
(2)A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: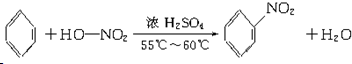 .
.
(4)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
(5)写出由D还原生成C的化学反应方程式:CH3CHO+H2 $\stackrel{催化剂}{→}$CH3CH2OH.
| A | B | C | D | E |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为:  | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. | ①相对分子质量比C少2; ②能由C氧化而成; | ①由C、H、O三种元素组成; ②球棍模型为: 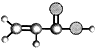 |
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学反应方程式
 .
.(2)A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 .
.(4)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为:CH2=CHCOOH+CH3CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOOCH2CH3+H2O.
(5)写出由D还原生成C的化学反应方程式:CH3CHO+H2 $\stackrel{催化剂}{→}$CH3CH2OH.