题目内容
将某Mg-Al合金放入足量的盐酸中,生成H2 的体积在标况下是2240ml;同质量的Mg-Al合金放入足量的NaOH溶液中生成H2 的体积在标况下是2016ml,则Mg、Al的质量之比是( )
| A、1:1 | B、6:1 |
| C、1:6 | D、4:27 |
考点:有关混合物反应的计算
专题:
分析:Mg、Al和HCl反应方程式为Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑,只有Al和NaOH溶液反应,反应方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,根据和NaOH反应放出的氢气计算m(Al),Al的质量相等,则Al和HCl生成的氢气与Al和NaOH生成的氢气量相等,则和HCl生成的氢气中除去Al生成的氢气剩余氢气是Mg和HCl生成的氢气,据此计算m(Mg).
解答:
解:只有Al和NaOH溶液反应,反应方程式为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,Al和NaOH反应生成n(H2)=
=0.09mol,根据2Al---3 H2得m(Al)=
×2×27g/mol=1.62g,
Al的质量相等,则Al和HCl生成的氢气与Al和NaOH生成的氢气量相等,所以Mg和盐酸反应生成n(H2)=
=0.01mol,根据Mg---H2得m(Mg)=
×1×24g/mol=0.24g,
所以m(Mg):m(Al)=0.24g:1.62g=4:27,
故选D.
| 2.016L |
| 22.4L/mol |
| 0.09mol |
| 3 |
Al的质量相等,则Al和HCl生成的氢气与Al和NaOH生成的氢气量相等,所以Mg和盐酸反应生成n(H2)=
| (2.24-2.016)L |
| 22.4L/mol |
| 0.01mol |
| 1 |
所以m(Mg):m(Al)=0.24g:1.62g=4:27,
故选D.
点评:本题考查混合物的计算,明确物质发生的反应是解本题关键,结合方程式进行计算即可,注意Mg、Al和稀盐酸都反应,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
要配制下列含有四种不同阴、阳离子的溶液,其中能配制成功的是( )
| A、Fe2+、OH-、NO3-、Cl- |
| B、Ca2+、H+、Cl-、HCO3- |
| C、Mg2+、Al3+、Cl-、SO42- |
| D、Na+、Ca2+、NO3-、CO32- |
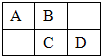 A、B、C、D为短周期元素,在周期表中所处的位置如图所示.A、D两元素的原子核外电子数之和等于B、C两元素的原子核外电子数之和.C元素的质子数是B元素的质子数的2倍.
A、B、C、D为短周期元素,在周期表中所处的位置如图所示.A、D两元素的原子核外电子数之和等于B、C两元素的原子核外电子数之和.C元素的质子数是B元素的质子数的2倍.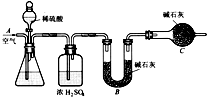
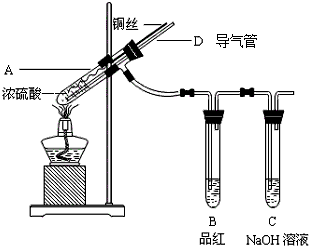 某同学为了探究铜与浓硫酸的反应,进行了如下实验.
某同学为了探究铜与浓硫酸的反应,进行了如下实验.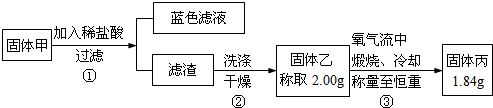
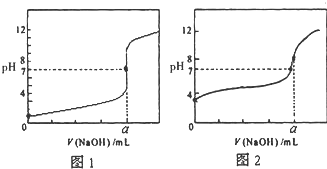 今有常温条件下A、B、C三种溶液,A为0.01mol?L-1的HCl溶液,B为0.01mol?L-1的CH3COOH溶液,C为0.01mol?L-1的NaOH溶液,回答下列问题:
今有常温条件下A、B、C三种溶液,A为0.01mol?L-1的HCl溶液,B为0.01mol?L-1的CH3COOH溶液,C为0.01mol?L-1的NaOH溶液,回答下列问题: