题目内容
在已处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明平衡移动的是( )
| A、反应混合物的浓度 |
| B、反应物的转化率 |
| C、正.逆反应速率 |
| D、反应混合物的压强 |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、如果两计量数相等,增大压强,反应体系的各物质的浓度变大,但平衡不移动,故A错误;
B、反应物的转化率的变化,说明化学平衡发生移动,故B正确;
C、正、逆反应速率变化量相等,但平衡不移动,故C错误;
D、两边气体的计量数相等,压强改变平衡不移动,故D错误;
故选B.
B、反应物的转化率的变化,说明化学平衡发生移动,故B正确;
C、正、逆反应速率变化量相等,但平衡不移动,故C错误;
D、两边气体的计量数相等,压强改变平衡不移动,故D错误;
故选B.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
两个体积相同的容器,一个盛有NO,一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的( )
| A、原子总数 | B、质子总数 |
| C、密度 | D、质量 |
化学兴趣小组设计如图实验装置.电解开始不久,铜电极附近溶液为无色,过了相当长时间后才呈蓝紫色.下列有关描述正确的是( )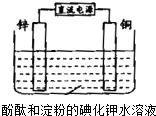

| A、电子由锌极流向铜极 |
| B、锌电极上的电极反应为:4OH--4e-═2H2O+O2↑ |
| C、铜电极实验现象的原因是生成的Cu2+和I-发生了反应 |
| D、将铜换成铁,电解开始后不久铁电极附近溶液即呈蓝紫色 |
在溶液中能大量共存,加入OH-有沉淀析出,加入H+有气体放出的是( )
| A、Mg2+、Na+、Cl-、CO32- |
| B、Fe3+、K+、SO42-、NO3- |
| C、H+、Al3+、OH-、NO3- |
| D、Na+、Ca2+、Cl-、HCO3- |