题目内容
10.某有机物的结构简式如图所示,有关该有机物的叙述正确的是( )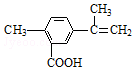
| A. | 在一定条件下,能发生取代、氧化、水解、酯化和加聚反应 | |
| B. | 该物质分子中最多可以有9个碳原子在同一平面上 | |
| C. | 1 mol该物质最多可与5mol H2发生加成反应 | |
| D. | 1 mol该物质完全氧化最多可消耗13 mol氧气 |
分析 由结构可知,分子中含-COOH、碳碳双键,结合羧酸、烯烃的性质来解答.
解答 解:A.含-COOH可发生酯化反应、取代反应,含碳碳双键可发生氧化、加聚反应,不能发生水解反应,故A错误;
B.苯环、碳碳双键为平面结构,且二者直接相连,则最多11个C原子共面,故B错误;
C.苯环、碳碳双键与氢气发生加成反应,则1 mol该物质最多可与4mol H2发生加成反应,故C错误;
D.分子中含11个C、12个H、2个O,1 mol该物质完全氧化最多可消耗1mol×(11+$\frac{12}{4}$-$\frac{2}{2}$)=13 mol氧气,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意羧酸、烯烃的性质应用,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案
相关题目
18.下列说法中正确的是( )
| A. | 1mol水的质量为18g/mol | |
| B. | 标准状况下,3.01×1023个CO2分子的质量为22g | |
| C. | 标准状况下,1mol任何物质体积约为22.4 L | |
| D. | 二氧化硫的摩尔质量是64 g |
15.下列与化学概念有关的说法正确的是( )
| A. | Na2O、CaO、Al2O3均为碱性氧化物 | |
| B. | 液溴不导电,所以液溴是非电解质 | |
| C. | 12C与13C的核外电子排布方式相同,化学性质相同 | |
| D. | 只含共价键的物质一定是共价化合物 |
2.下列实验的反应原理用离子方程式表示正确的是( )
| A. | 明矾净水:Al3++3H2O=Al(OH)3↓+3H+ | |
| B. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| C. | 用CuCl2溶液做导电实验,灯泡发光:CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu2++2C1- | |
| D. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O |
19.下列说法不正确的是( )
| A. | 丁达尔效应可用于鉴别胶体和溶液 | |
| B. | 胶体粒子的直径在1~100 nm之间 | |
| C. | 胶体一定是混合物 | |
| D. | 将FeCl3稀溶液溶于冷水即可制得Fe(OH)3胶体 |

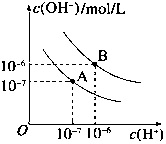 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: