题目内容
用NA 表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、98克H2SO4和H3PO4 含有的氧原子数均为4NA. |
| B、1L1mol?L-1 的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA |
| C、33.6LNO2 溶解于足量的水中得到的硝酸溶液,溶液中NO3-数目为NA |
| D、32克铜发生氧化还原反应,一定失去NA 个电子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、H2SO4和H3PO4 的摩尔质量均为98g/mol;
B、硫酸和高氯酸溶液中除了H2SO4和HClO4中含有氧原子,溶剂水中也含有氧原子;
C、NO2 所处的状态不明确;
D、铜发生氧化反应后,价态可能变为+1价或+2价.
B、硫酸和高氯酸溶液中除了H2SO4和HClO4中含有氧原子,溶剂水中也含有氧原子;
C、NO2 所处的状态不明确;
D、铜发生氧化反应后,价态可能变为+1价或+2价.
解答:
解:A、H2SO4和H3PO4 的摩尔质量均为98g/mol,故98gH2SO4和H3PO4 的物质的量为1mol,而H2SO4和H3PO4 均含4个氧原子,故1molH2SO4和H3PO4 中均含4mol氧原子,故A正确;
B、硫酸和高氯酸溶液中除了H2SO4和HClO4中含有氧原子,溶剂水中也含有氧原子,故两溶液中含有的氧原子数大于4NA,故B错误;
C、NO2 所处的状态不明确,不一定是标况,故33.6L二氧化氮的物质的量不一定是1.5mol,故生成的硝酸不一定是1mol,故C错误;
D、32g铜的物质的量n=
=0.5mol,而铜发生氧化反应后价态可能变为+1价或+2价,故0.5mol铜失去的电子的物质的量可能为0.5mol或1mol,故D错误.
故选A.
B、硫酸和高氯酸溶液中除了H2SO4和HClO4中含有氧原子,溶剂水中也含有氧原子,故两溶液中含有的氧原子数大于4NA,故B错误;
C、NO2 所处的状态不明确,不一定是标况,故33.6L二氧化氮的物质的量不一定是1.5mol,故生成的硝酸不一定是1mol,故C错误;
D、32g铜的物质的量n=
| 32g |
| 64g/mol |
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
常温下,将Na2CO3和NaHCO3的混合物[设
=a,0<a≤3]溶于水得到稀溶液,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| n(Na2CO3) |
| n(NaHCO3) |
| A、若a=1,则:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| B、若a=2,则:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C、a为任意值时:c(Na+)+c(H+)=c(HCO32-)+2c(CO32-)+c(OH-) |
| D、若满足:3c(H+)+2c(HCO3-)+5c(H2CO3)=3c(OH-)+c(CO32-),则可确定a=3 |
将0.2mol AgNO3、0.4mol Cu(NO3)2和0.6mol KCl溶于水配成100mL溶液,用惰性电极电解一段时间后,在一极上析出0.3mol Cu,此时,另一极上的气体体积(标准状况)为( )
| A、4.48 L |
| B、5.6 L |
| C、6.72 L |
| D、7.8 L |
测得室温下0.1mol?L-1的某酸HA溶液的PH=3,下列叙述错误的是( )
| A、HA是弱酸 |
| B、若升高温度,溶液的PH增大 |
| C、此酸的电离平衡常数约为10-5 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的108倍 |
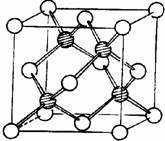 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有
冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有
 X溶液与Y溶液反应的离子方程式为
X溶液与Y溶液反应的离子方程式为