题目内容
2.下列有关金属的说法中,正确的是( )①钠着火可用水扑灭; ②铝在空气中不易被腐蚀,所以铝是不活泼金属; ③生铁在潮湿的空气中可发生吸氧腐蚀; ④人体缺钙会引起骨质疏松、缺铁会引起贫血; ⑤青铜、不锈钢、硬铝都是合金; ⑥Al和Fe在一定条件下能与某些氧化物反应.
| A. | ①②⑤ | B. | ②③⑤ | C. | ③④⑤⑥ | D. | 全都正确 |
分析 ①钠和水发生剧烈反应生成氢氧化钠和氢气;
②根据铝是活泼金属,空气中耐腐蚀是表面形成了稳定的氧化物分析;
③原电池中,作原电池负极的金属易失电子而被腐蚀,则作原电池正极的金属被保护,铁在潮湿空气中发生腐蚀,其负极反应是Fe-2e-=Fe2+;
④人体缺钙会引起骨质疏松、缺铁会引起贫血,人体缺钙会引起骨质疏松、缺铁会引起贫血;
⑤根据青铜、不锈钢、硬铝的成分和合金的概念分析判断;
⑥Al和Fe在一定条件下都能与某些氧化物反应,如铝热反应、Fe与水蒸气反应.
解答 解:①钠和水发生剧烈反应生成氢氧化钠和氢气,燃烧更旺,应用沙土盖灭,故①错误;
②铝是活泼金属,在空气中耐腐蚀是因为表面形成了一层氧化铝保护膜,阻止反应进行,在空气中耐腐蚀,故②错误;
③铁在潮湿空气中发生腐蚀,其负极反应是Fe-2e-=Fe2+,正极是氧气得到电子发生还原反应生成氢氧根离子,发生的是吸氧腐蚀,故③正确;
④人体缺钙会引起骨质疏松、缺铁会引起贫血,故④正确;
⑤青铜是铜锡合金、不锈钢是铁铬、镍合金、硬铝是铝硅、镁等形成的合金,故⑤正确;
⑥Al和Fe在一定条件下都能与某些氧化物反应,如铝热反应、Fe与水蒸气反应生成四氧化三铁与氢气,故⑥正确;
故选C.
点评 本题题目综合性较大,涉及元素化合物性质、金属腐蚀、原电池反应、合金等,题目难度中等,旨在考查学生对基础知识的全面掌握情况.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
12.能正确表示下列反应离子方程式的是( )
| A. | CuCl2溶液中加入少量氨水:Cu2++2OH-═Cu(OH)2↓ | |
| B. | 向酸性KMnO4溶液中通入SO2:3SO2+2MnO4-+4OH-═2MnO2↓+3SO42-+2H2O | |
| C. | 向CuSO4溶液中加Na2O2:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ | |
| D. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- |
10.下列实验操作或实验事故处理正确的是( )
| A. | 实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 实验时手指不小心沾上苯酚,立即用70℃以上的热水清洗 | |
| D. | 实验室检验卤代烃时,试剂只需用NaOH的水溶液和AgNO3溶液即可 |
7.下列表示对应化学反应的离子方程式正确的是( )
| A. | 钠与CuSO4溶液反应:2Na+Cu=Cu↓+2Na+ | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
14.下列离子方程式书写正确的是( )
| A. | 在氯化铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3 | |
| B. | 在澄清石灰水中通入过量CO2:OH-+CO2=HCO3- | |
| C. | 在碳酸氢钙溶液中加入过量NaOH溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| D. | 碳酸钡中加入稀硫酸:BaCO3+2H+=Ba2++CO2↑+H2O |
11.下列关于元素周期表的说法正确的是( )
| A. | 过渡元素全部都是副族元素 | |
| B. | 短周期共有32 种元素 | |
| C. | 科学研究时,经常在过渡元素中寻找耐高温、耐腐蚀的合金材料 | |
| D. | 元素周期表共七个横行代表七个周期,18 个纵横代表18 个族 |
8. Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)①
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果偏小(填“偏大”、“偏小”或“无影响”)
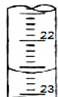
(3)右图是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)根据下列数据:请计算待测盐酸溶液的浓度:0.2mol/L
Ⅱ按要求回答下列问题:
(5)某温度时,水的离子积常数KW=10-13,将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合,设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=10:1
(6)已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17.则AgX、AgY、AgZ三者的溶解度(mol/L)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:s(AgX)>s(AgY)>s(AgZ);若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)减小(填“增大”“减小”或“不变”).
 Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
Ⅰ:某学生用0.20mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)①
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果偏小(填“偏大”、“偏小”或“无影响”)
(3)右图是某次滴定时的滴定管中的液面,其读数为22.60mL
(4)根据下列数据:请计算待测盐酸溶液的浓度:0.2mol/L
| 滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 4.00 | 24.00 |
| 第三次 | 20.00 | 2.00 | 24.10 |
(5)某温度时,水的离子积常数KW=10-13,将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合,设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=10:1
(6)已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10-10,Ksp(AgY)=1.0×10-12,Ksp(AgZ)=8.7×10-17.则AgX、AgY、AgZ三者的溶解度(mol/L)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:s(AgX)>s(AgY)>s(AgZ);若向AgY的饱和溶液中加入少量的AgX固体,则c(Y-)减小(填“增大”“减小”或“不变”).
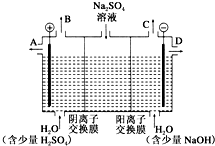 芒硝化学式为Na2SO4•10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念.
芒硝化学式为Na2SO4•10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念. .
. .
.