题目内容
18.常温下,下列各组离子在指定环境下能大量共存的是( )| A. | pH=1的溶液中:Na+、K+、SO32-、MnO4- | |
| B. | pH=7的溶液中:Na+、Al3+、Cl-、SO42- | |
| C. | pH>12的溶液中:Na+、K+、SO42-、AlO2- | |
| D. | pH=0的溶液中:Na+、K+、NO3-、ClO- |
分析 A.pH=1的溶液呈酸性;
B.pH=7的溶液呈中性,水解的离子不能大量共存;
C.pH>12的溶液呈碱性;
D.pH=0的溶液呈酸性.
解答 解:A.pH=1的溶液呈酸性,酸性条件下SO32-、MnO4-发生氧化还原反应而不能大量共存,故A错误;
B.pH=7的溶液呈中性,Al3+水解呈酸性,不能大量共存,故B错误;
C.pH>12的溶液呈碱性,碱性条件下离子之间不发生任何反应,可大量共存,故C正确;
D.pH=0的溶液呈酸性,酸性条件下ClO-不能大量共存,故D错误.
故选C.
点评 本题考查离子的共存,为高考高频考点,侧重复分解反应、氧化还原反应的离子共存的考查,注意把握习题中的信息及常见离子之间的反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.0.2mol•L-1的下列溶液导电能力最强的是( )
| A. | H2SO4(aq) | B. | HCl(aq) | C. | Fe2(SO4)3(aq) | D. | CuSO4(aq) |
3.柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源.液体矿床以钾矿为主,伴生着镁、溴等多种矿产.某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如图1流程:
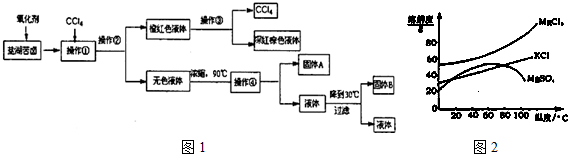
请根据以上流程,回答相关问题:
(1)操作②的所需的主要仪器是分液漏斗.
(2)参照图2溶解度曲线,得到的固体A的主要成分是MgSO4(填化学式).
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
【有关资料】
【设计除杂过程】
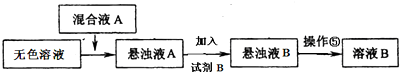
①已知试剂B是K2CO3溶液,则混合液A的主要成分是Ba(OH)2(或BaCl2和KOH)(填化学式).
【获取纯净氯化钾】
②对溶液B加热并不断滴加l mol•L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是加盐酸调节至pH=5目的是除去未反应的OH-和CO32-.
③将溶液C倒入 蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到出现较多晶体,剩余较少水时时(填现象),停止加热.
【问题讨论】
④进行操作⑤中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶液B中Mg2+物质的量浓度为1.6×10-7mol/L.

请根据以上流程,回答相关问题:
(1)操作②的所需的主要仪器是分液漏斗.
(2)参照图2溶解度曲线,得到的固体A的主要成分是MgSO4(填化学式).
(3)同学甲提出一些新的方案,对上述操作②后无色溶液进行除杂提纯,其方案如下:
【有关资料】
| 化学式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |

①已知试剂B是K2CO3溶液,则混合液A的主要成分是Ba(OH)2(或BaCl2和KOH)(填化学式).
【获取纯净氯化钾】
②对溶液B加热并不断滴加l mol•L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是加盐酸调节至pH=5目的是除去未反应的OH-和CO32-.
③将溶液C倒入 蒸发皿中,加热蒸发并用玻璃棒不断搅拌,直到出现较多晶体,剩余较少水时时(填现象),停止加热.
【问题讨论】
④进行操作⑤中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶液B中Mg2+物质的量浓度为1.6×10-7mol/L.
2.下列说法正确的是( )
| A. | 将25gKCl溶液蒸干得到5gKCl固体,则原溶液中溶质的质量分数为20% | |
| B. | 某物质中只含有一种元素,则该物质一定是纯净物 | |
| C. | 只有一种元素的阳离子和一种元素的阴离子构成的物质一定是纯净物 | |
| D. | 盐形成的溶液中,既不能电离出H+,也不能电离出OH- |
3.将N2和O2混合气体置于一个密闭容器中,经电火花放电后,恢复到原来的温度和压强,发现气体体积无变化,则原来混合气体中N2和O2的体积比是( )
| A. | 1:1 | B. | <1:1 | C. | ≥1:1 | D. | 任意比 |
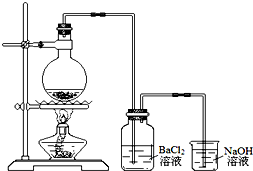 某学习小组探究铜跟浓硫酸反应的情况.取6.4g铜片和10mL 18mol•L-1的浓硫酸放在圆底烧瓶中,按如图所示装置进行实验.
某学习小组探究铜跟浓硫酸反应的情况.取6.4g铜片和10mL 18mol•L-1的浓硫酸放在圆底烧瓶中,按如图所示装置进行实验.