题目内容
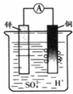
如右图装置所示,铜片上发生的反应为
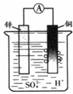
A.Zn2+ + 2e— === Zn B.2H+ + 2e— === H2↑
C.Zn - 2e— === Zn2+ D.Cu2+ + 2e— === Cu
【答案】
B
【解析】该装置是原电池,因为锌比铜活泼,所以锌是负极,失去电子,被氧化。铜是正极,溶液中的氢离子在正极得到电子,被还原,生成氢气,所以答案是B。

练习册系列答案
相关题目
如右图装置所示,铜片上发生的反应为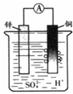
| A.Zn2+ + 2e—===Zn | B.2H+ + 2e—===H2↑ |
| C.Zn - 2e—===Zn2+ | D.Cu2+ + 2e—===Cu |
 如右图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.下列叙述正确的是( )
如右图所示,把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池.下列叙述正确的是( )