题目内容
12.在一定温度下,10L密闭容器中加入5molSO2、3molO2,反应达到平衡时有3molSO2发生了反应.试填写下列空格:(1)O2的转化率为50%.
(2)平衡时容器内气体总物质的量为6.5mol.
(3)平衡时体系中SO3的百分量(体积分数)为46.2%.(保留一位小数)
(4)若反应前容器内压强为p1,则平衡时容器内压强为0.8p1.(用p1表示,保留一位小数)
分析 加入5molSO2和3molO2,当反应达到平衡时,有3molSO2发生反应,则
2SO2(g)+O2 (g)?2SO3(g),
起始:5mol 3mol 0
转化:3mol 1.5mol 3mol
平衡:2mol 1.5mol 3mol
以此解答该题.
解答 解:加入5molSO2和3molO2,当反应达到平衡时,有3molSO2发生反应,则
2SO2(g)+O2 (g)?2SO3(g),
起始:5mol 3mol 0
转化:3mol 1.5mol 3mol
平衡:2mol 1.5mol 3mol
(1)O2的转化率为$\frac{1.5}{3}×100%$=50%,故答案为:50%;
(2)平衡时容器内气体总物质的量为2mol+1.5mol+3mol=6.5mol,故答案为:6.5;
(3)平衡时体系中SO3的百分量(体积分数)为$\frac{3}{6.5}×100%$=46.2%,故答案为:46.2%;
(4)气体的物质的量之比等于压强比,若反应前容器内压强为p1,则平衡时容器内压强为$\frac{6.5}{8}$×p1=0.8p1,故答案为:0.8p1.
点评 本题考查化学平衡的计算,题目难度中等,注意三段式计算方法的运用,明确转化率、物质的量浓度等物理量的概念及表达式,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
20.已知有反应:2A(g)+B(g)$\frac{\underline{\;催化剂\;}}{\;}$3C(g);△H<0,在恒容的密闭容器中,通入A和B气体,反应达到平衡后,若仅改变图中x的值,则y随x变化趋势合理的是( )
| 选项 | X | Y | 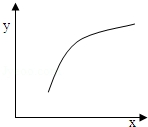 |
| A | 温度 | 容器内混合气体的密度 | |
| B | A的物质的量 | B的转化率 | |
| C | 催化剂的质量 | C的体积分数 | |
| D | 加入Ar的物质的量 | 逆反应速率 |
| A. | A | B. | B | C. | C | D. | D |
7.N2O5是一种新型硝化剂,在一定温度下向密闭容器中通入N2O5气体,发生如下反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.部分实验数据见表:
下列说法中不正确的是( )
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500 s内N2O5分解速率为296×10-3mol•L-1•s-1 | |
| B. | 该温度下的反应平衡时N2O5的转化率为29.6% | |
| C. | 1000s后,其它条件不变,将容器的体积压缩到原来的$\frac{1}{2}$,则c(N2O5)<5.00mol/L | |
| D. | 反应达平衡后,其他条件不变,升高温度平衡常数将增大 |
4.已知:CO(g)+2H2(g)?CH3OH(g)△H<0.其它条件不变的情况下,下列有关该反应的说法中正确的是( )
| A. | 升高温度可以提高CO的转化率 | |
| B. | 加入催化剂能提高CO的转化率 | |
| C. | 缩小反应器容积可以使平衡正向移动 | |
| D. | 再充入适量H2,该反应平衡常数的数值会增大 |
1.取20.00mL 0.50mol•L-1NaOH溶液,恰好将未知浓度的H2SO4溶液20.00mL滴定至终点,下列说法正确的是( )
| A. | 该实验不需要指示剂 | |
| B. | 用量筒量取上述硫酸的体积 | |
| C. | H2SO4的浓度为1.00 mol•L-1 | |
| D. | 参加反应的H+和OH-的物质的量相等 |
2.下列热化学方程式正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ•mol-1(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3 kJ•mol-1(中和热) | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1(反应热) | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=571.6kJ•mol-1(反应热) |
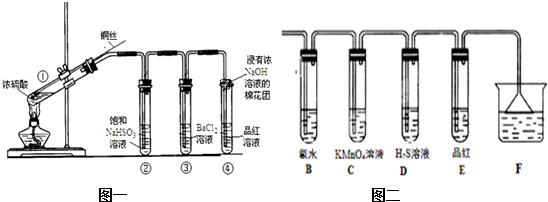
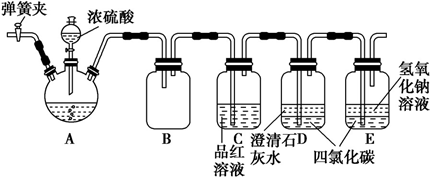
 某课外小组利用下列装置,对浓硫酸与乙醇反应的可能产物进行了如下探究.
某课外小组利用下列装置,对浓硫酸与乙醇反应的可能产物进行了如下探究.