题目内容
下列离子方程式正确的是( )
| A、铜片加入稀硝酸中:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O |
| B、向小苏打溶液中加入醋酸:HCO3-+H+═CO2↑+H2O |
| C、向HI溶液中加入Fe(OH)3固体:Fe(OH)3+3H═Fe3++3H2O |
| D、向MgSO4溶液中加入Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.铜片加入稀硝酸生成铜离子、NO和水;
B.醋酸是弱电解质,要写化学式;
C.碘离子能被三价铁离子氧化为碘单质;
D.向MgSO4溶液中加入Ba(OH)2溶液生成硫酸钡沉淀和氢氧化镁沉淀.
B.醋酸是弱电解质,要写化学式;
C.碘离子能被三价铁离子氧化为碘单质;
D.向MgSO4溶液中加入Ba(OH)2溶液生成硫酸钡沉淀和氢氧化镁沉淀.
解答:
解:A.铜片加入稀硝酸生成铜离子、NO和水,其离子方程式为:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O,故A正确;
B.醋酸是弱电解质,要写化学式,则向小苏打溶液中加入醋酸的离子方程式为:HCO3-+CH3COOH═CH3COO-+CO2↑+H2O,故B错误;
C.碘离子能被三价铁离子氧化为碘单质,则向HI溶液中加入Fe(OH)3固体:2Fe(OH)3+6H++2I-═2Fe3++6H2O+I2,故C错误;
D.向MgSO4溶液中加入Ba(OH)2溶液生成硫酸钡沉淀和氢氧化镁沉淀,其离子方程式为:Mg2++SO42-+Ba2++2OH-=Mg(OH)2↓+BaSO4↓,故D错误.
故选A.
B.醋酸是弱电解质,要写化学式,则向小苏打溶液中加入醋酸的离子方程式为:HCO3-+CH3COOH═CH3COO-+CO2↑+H2O,故B错误;
C.碘离子能被三价铁离子氧化为碘单质,则向HI溶液中加入Fe(OH)3固体:2Fe(OH)3+6H++2I-═2Fe3++6H2O+I2,故C错误;
D.向MgSO4溶液中加入Ba(OH)2溶液生成硫酸钡沉淀和氢氧化镁沉淀,其离子方程式为:Mg2++SO42-+Ba2++2OH-=Mg(OH)2↓+BaSO4↓,故D错误.
故选A.
点评:本题考查离子反应方程式书写,把握发生的反应及离子反应的书写方法为解答的关键,题目难度不大.

练习册系列答案
相关题目
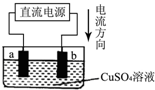 化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )
化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极.则下列说法错误的是( )| A、a是电解池的阴极、b是电解池的阳极 |
| B、b电极上的电极反应为:4OH--4e-=2H2O+O2↑ |
| C、通电一段时间后,溶液的PH减小 |
| D、通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入适量的CuSO4 |
已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列判断正确的是( )
| A、元素金属性:B>A;元素非金属性:D>C |
| B、原子半径:A>B>C>D |
| C、离子半径:D(n+1)->C n->B (n+1)+>A n+ |
| D、原子序数:b>a>c>d |
下列说法中正确的是( )
| A、摩尔是表示物质质量的单位 |
| B、10g氟化氢含有0.5molHF分子 |
| C、1g氢气的物质的量是1mol |
| D、物质的摩尔质量等于其式量 |
下列说法正确的是( )
| A、在化学反应中发生物质变化的同时,一定发生能量变化 |
| B、△H>0表示放热反应,△H<0表示吸热反应 |
| C、△H的大小与热化学方程式中化学计量数无关 |
| D、生成物释放的总能量大于反应物吸收的总能量时,△H>0 |
下列物质中含有共价键的离子化合物是( )
①MgF2 ②Na2O2 ③NaOH ④CO2 ⑤NH4Cl ⑥H2O2 ⑦N2.
①MgF2 ②Na2O2 ③NaOH ④CO2 ⑤NH4Cl ⑥H2O2 ⑦N2.
| A、②③④⑤ | B、②③⑤ |
| C、①②③⑤ | D、①③⑤⑥ |
经测定甲醇和环己烷组成混合物中,氧的质量分数为8%,则此混合物中氢的质量分数为( )
| A、78% | B、28% |
| C、14% | D、13% |
下列说法或有关化学用语表达正确的是( )
| A、二氧化碳的结构式:O-C-O |
B、Cl-的结构示意图: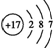 |
| C、乙醇的结构简式:CH3CH2OH |
| D、过氧化氢(D2O2)的相对分子质量为34 |
氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s)═2NaNO3(s)+2NO(g)+Cl2(g),△H在恒温条件下,向2L恒容密闭容器中加入0.4mol NO2和0.2mol NaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为α.下列叙述中正确的是( )
| A、10min内NO浓度变化表示的速率v(NO)=0.01 mol?L-1?min-1 |
| B、若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率大于α |
| C、若升高温度,平衡逆向移动,则该反应的△H>0 |
| D、若起始时向容器中充入NO2(g) 0.1 mol、NO(g)0.2 mol和Cl2(g)0.1 mol(固体物质足量),则反应将向逆反应方向进行 |