题目内容
6.下列反应的离子方程式正确的是( )| A. | 铁与稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 氢氧化铁溶液与盐酸反应:OH-+H+═H2O | |
| C. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu | |
| D. | 氢氧化钡溶液与稀硫酸反应:H++SO42-+OH-+Ba2+═BaSO4↓+H2O |
分析 A、铁与稀硝酸反应生成硝酸铁、水以及一氧化氮;
B、氢氧化铁溶液与盐酸反应生成氯化铁和水;
C、锌与硫酸铜溶液反应生成硫酸锌和金属铜;
D、氢氧化钡溶液与稀硫酸反应生成硫酸钡和水.
解答 解:A、铁与稀硝酸反应生成硝酸铁、水以及一氧化氮:Fe+4H++NO3-=Fe3++NO↑+2H2O,故A错误;
B、氢氧化铁溶液与盐酸反应生成氯化铁和水:Fe(OH)3+3H+═Fe3++3H2O,Fe(OH)3不拆,故B错误;
C、锌与硫酸铜溶液反应生成硫酸锌和金属铜,即Zn+Cu2+═Zn2++Cu,故C正确;
D、氢氧化钡溶液与稀硫酸反应生成硫酸钡和水,即2H++SO42-+2OH-+Ba2+═BaSO4↓+2H2O,离子个数符合物质的配比关系,故D错误.
故选C.
点评 本题考查离子反应方程式的正误判断,明确发生的化学反应及离子反应的书写方法即可解答,离子方程式的书写要遵循电荷守恒、原子守恒、转移电子守恒,注意有些化学反应还与反应物的量有关,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列温室气体中,和 CO2一样,既是非极性分子,所有的原子又都达到8电子稳定结构的是( )
| A. | N2O | B. | CF2=CF2 | C. | CCl2F2 | D. | SF6 |
1.用锌粒与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
| A. | 加热 | B. | 滴加少量硫酸铜溶液 | ||
| C. | 不用铁片,改用铁粉 | D. | 加少量浓硝酸 |
11.下列实验操作或事故处理方法正确的是( )
| A. | 金属Na着火,立即用水扑灭 | |
| B. | 做蒸馏实验时,应使温度计水银球位于蒸馏烧瓶支管口处 | |
| C. | 衣服沾上大量浓氢氧化钠溶液,需将此衣服浸泡在盛水的盆中 | |
| D. | 测试某溶液的pH时,先用水润湿pH试纸,再将待测液滴到pH试纸上 |
15.氯的含氧酸根离子有ClO-、ClO2-、ClO3-、ClO4-等,有关它们的下列说法正确的是( )
| A. | ClO-中氯元素显+1价,具有很强的还原性 | |
| B. | 这些离子结合H+的能力,ClO4-最强 | |
| C. | ClO3-是NO3-的等电子体,其空间构型为平面三角形 | |
| D. | ClO2-、ClO3-、ClO4-中的氯原子都采取sp3杂化,离子中相邻两个Cl-O键间键角依次增大 |
 碳元素形成的单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔触的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为KC8.
碳元素形成的单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔触的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图所示,该物质的化学式为KC8.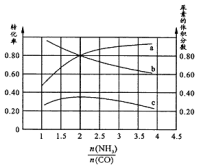 用CO合成尿素的反应为:2NH3(g)+CO(g)?CO(NH2)2(g)+H2(g)△H<0.
用CO合成尿素的反应为:2NH3(g)+CO(g)?CO(NH2)2(g)+H2(g)△H<0.