题目内容
在一个不传热的固定容积的密闭容器中,可逆反应:N2+3H2═2NH3,达到平衡的标志是( )
①反应速率v(N2):v(H2):v(NH3)=1:3:2
②各组分的物质的量浓度不再改变
③体系的压强不再发生变化
④混合气体的密度不变
⑤体系的温度不再发生变化
⑥2V(N2)正=V(NH3)逆
⑦单位时间内3mol H-H断键反应同时2mol N-H也断键反应.
①反应速率v(N2):v(H2):v(NH3)=1:3:2
②各组分的物质的量浓度不再改变
③体系的压强不再发生变化
④混合气体的密度不变
⑤体系的温度不再发生变化
⑥2V(N2)正=V(NH3)逆
⑦单位时间内3mol H-H断键反应同时2mol N-H也断键反应.
| A、①、②、③、⑤、⑥ |
| B、②、③、⑤、⑥ |
| C、②、③、⑤、⑥、⑦ |
| D、②、③、④、⑥、⑦ |
考点:化学平衡状态的判断
专题:
分析:化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量不变,注意化学方程式的特点,反应物的化学计量数之和大于生成物的化学计量数之和,反应放热等特点.
解答:
解:①.无论是否达到平衡状态,化学反应速率之比都等于化学计量数之比,故错误;
②.当反应达到平衡状态时,各组分的物质的量浓度不再改变,故正确;
③.反应前后气体的化学计量数之和不相等,当达到平衡状态时,压强不变,故正确;
④.反应前后气体的质量不变,容器的体积不变,无论是否达到平衡状态,气体的密度都不变,不能作为判断是否达到平衡状态的依据,故错误;
⑤.反应达到平衡状态时,反应物的物质的量不再发生改变,体系的温度不变,故正确;
⑥.2υ(N2) (正反应)=υ(NH3)(逆反应),说明正逆反应速率相等,达到平衡状态,故正确;
⑦.单位时间内 3molH-H键断裂的同时有6molN-H键断裂,说明正逆反应速率相等,达到平衡状态,所以单位时间内3mol H-H断键反应同时2mol N-H也断键反应时反应没有达到平衡状态,故错误.
故选B.
②.当反应达到平衡状态时,各组分的物质的量浓度不再改变,故正确;
③.反应前后气体的化学计量数之和不相等,当达到平衡状态时,压强不变,故正确;
④.反应前后气体的质量不变,容器的体积不变,无论是否达到平衡状态,气体的密度都不变,不能作为判断是否达到平衡状态的依据,故错误;
⑤.反应达到平衡状态时,反应物的物质的量不再发生改变,体系的温度不变,故正确;
⑥.2υ(N2) (正反应)=υ(NH3)(逆反应),说明正逆反应速率相等,达到平衡状态,故正确;
⑦.单位时间内 3molH-H键断裂的同时有6molN-H键断裂,说明正逆反应速率相等,达到平衡状态,所以单位时间内3mol H-H断键反应同时2mol N-H也断键反应时反应没有达到平衡状态,故错误.
故选B.
点评:本题考查考查化学平衡状态的判断,题目难度中等,本题注意不传热的固定容积的密闭容器,⑤为易错点,做题时注意把握化学方程式的特征.

练习册系列答案
相关题目
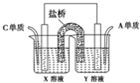
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )

| A、甲池中,b电极是负极 |
| B、a电极的电极反应式C2H5OH+16OH--12e-═2CO32-+11H2O |
| C、一段时间后,用湿润淀粉KI试纸靠近乙池d电极变蓝放电 |
| D、乙池在反应前后溶液的pH不变充电 |
下列反应属于吸热反应的是( )
| A、镁与稀盐酸反应 |
| B、CO燃烧生成CO2 |
| C、生石灰溶于水 |
| D、氢氧化钙与氯化铵晶体混合 |
原子序数依次增大的X、Y、Z、R、W、T六种前20号元素,X、Y原子的最外层电子数与其电子层数相等,Y、T位于同族,R最外层电子数是次外层的3倍,W无正价,甲的化学式为ZX3,是一种刺激性气味的气体,乙是由X、Z、W组成的盐.下列说法正确的是( )
| A、由X、Z、W组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 |
| B、气态氢化物的稳定性:W<R<Z |
| C、原子半径:W<Z<Y,而简单离子半径:Y<Z<W |
| D、ZR2、TR2两化合物中R的化合价相同 |
主族元素在周期表的位置,取决于元素原子的( )
| A、相对原子质量和核电荷数 |
| B、电子层数和最外层电子数 |
| C、电子层数和质量数 |
| D、金属性和非金属性的强弱 |
 A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大.A、D同主族;B、D、E三种元素原子的最外层电子数之和为9.又知B、D、E分别与A、C两元素形成的三种化合物X、Y、Z之间能相互发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M,1mol M中含有42mol电子.回答下列问题:
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大.A、D同主族;B、D、E三种元素原子的最外层电子数之和为9.又知B、D、E分别与A、C两元素形成的三种化合物X、Y、Z之间能相互发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M,1mol M中含有42mol电子.回答下列问题: