题目内容
某溶液中可能含有I-、NH4+、Cu2+、SO32-,向溶液中加入足量的溴水,反应后溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-.
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-.
| A、①② | B、①②③ |
| C、②③④ | D、①③ |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:还原性SO32->I-,溶液中加入足量溴水,溶液仍呈无色,说明一定含有SO32-,溶液中不可能含有I-离子,反应后溶液呈无色,说明不含Cu2+离子,根据溶液电中性,进一步判断其它离子是否存在.
解答:
解:溴水具有强氧化性,可与I-、SO32-发生氧化还原反应,溶液中加入足量溴水,溶液仍呈无色,说明一定含有SO32-,不含有I-离子,含Cu2+离子的溶液呈蓝色,反应后溶液无色说明不含铜离子,根据溶液呈电中性可知,溶液中含有铵根离子,故正确的有①②③,
故选B.
故选B.
点评:本题考查离子的检验,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及反应的现象,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列对有关实验的描述不正确的是( )
| A、在浓氨水中加入生石灰可以制取少量的NH3 | ||||
B、用惰性电极电解熔融NaCl:2Cl-+2H2O
| ||||
| C、氯水和活性炭使红墨水褪色,能用同一原理解释 | ||||
| D、浓硫酸和浓盐酸长期暴露在空气中浓度都会降低 |
在常温常压下,向100mL CH4和Ar的混合气体中通入400mL O2,点燃使其完全反应,最后在相同条件下得到干燥气体450mL,则反应前混合气体中CH4和Ar的物质的量之比为( )
| A、1:4 | B、1:3 |
| C、1:2 | D、1:1 |
有两种金属组成的混合物粉末10g与足量的稀盐酸反应,生成11.2L(标况)H2,则该混合物的组成可能是( )
| A、Fe、Zn |
| B、Fe、Cu |
| C、Cu、Mg |
| D、Al、Fe |
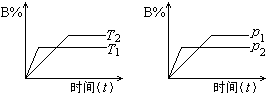 已知某可逆反应:mA(g)+nB(g)?pC(g)+Q(Q为热量变化).在密闭容器中进行,如图所示,反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)+Q(Q为热量变化).在密闭容器中进行,如图所示,反应在不同时间t,温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )| A、T1<T2,p1>p2,m+n>p,Q<0 |
| B、T1>T2,p2>p1,m+n>p,Q<0 |
| C、T1>T2,p2>p1,m+n<p,Q<0 |
| D、T1>T2,p1<p2,m+n>p,Q>0 |
下列叙述不正确的是( )
| A、在基态多电子的原子中,最易失去的电子能量最高电离能也最小 |
| B、锗的第一电离能高于碳而电负性低于碳 |
| C、PH3分子呈三角锥形,沸点比NH3低 |
| D、SiF4和SO32-的中心原子均为sp3杂化 |
