��Ŀ����
��һ���¶��£���2molA��2molB������������ij2L���ܱ������У��������·�Ӧ��3A��g��+B��g��?2C��g��+2D��g����2minĩ��Ӧ�ﵽƽ�⣬����0.8molD������д���пհף�
��1��B��ƽ��Ũ��Ϊ ��
��2��A��ת����Ϊ ��
��3����C��ʾ��ƽ����Ӧ����Ϊ ��
��4�������С��Ӧ������������¶Ȳ��䣩��ʹѹǿ������ƽ����ϵ��C�����ʵ���Ũ�� ��C���������� �������ڻ��������ܶ� ����������ƽ����Է������� ���������������С�����䡱��
��1��B��ƽ��Ũ��Ϊ
��2��A��ת����Ϊ
��3����C��ʾ��ƽ����Ӧ����Ϊ
��4�������С��Ӧ������������¶Ȳ��䣩��ʹѹǿ������ƽ����ϵ��C�����ʵ���Ũ��
���㣺��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
���������ݻ�ѧƽ������ʽ��ʽ����
3A��g��+B��g��?2C��g��+2D��g��
��ʼ����mol�� 2 2 0 0
�仯����mol 1.2 0.4 0.8 0.8
ƽ������mol�� 0.8 1.6 0.8 0.8
��1��ƽ��Ũ��=
��
��2��ת����=
��100%��
��3����Ӧ����=
����õ���
��4�������С��Ӧ������������¶Ȳ��䣩��ʹѹǿ����ƽ�������ʵ�Ũ������Ӧǰ�������������ƽ�ⲻ�䣬����������������䣬�ܶȲ��䣬ƽ��Ħ������=
����Ӧǰ�����ʵ������䣬�����������������
3A��g��+B��g��?2C��g��+2D��g��
��ʼ����mol�� 2 2 0 0
�仯����mol 1.2 0.4 0.8 0.8
ƽ������mol�� 0.8 1.6 0.8 0.8
��1��ƽ��Ũ��=
| n |
| V |
��2��ת����=
| ������ |
| ��ʼ�� |
��3����Ӧ����=
| ��c |
| ��t |
��4�������С��Ӧ������������¶Ȳ��䣩��ʹѹǿ����ƽ�������ʵ�Ũ������Ӧǰ�������������ƽ�ⲻ�䣬����������������䣬�ܶȲ��䣬ƽ��Ħ������=
| ���� |
| ���ʵ��� |
���
�⣺���ݻ�ѧƽ������ʽ��ʽ����
3A��g��+B��g��?2C��g��+2D��g��
��ʼ����mol�� 2 2 0 0
�仯����mol 1.2 0.4 0.8 0.8
ƽ������mol�� 0.8 1.6 0.8 0.8
��1��B��ƽ��Ũ��=
=
=0.8mol/L��
�ʴ�Ϊ��0.8mol/L��
��2��A��ת����=
��100%=
��100%=60%��
�ʴ�Ϊ��60%��
��3����C��ʾ��ƽ����Ӧ����=
=
=0.2mol/L?min��
�ʴ�Ϊ��0.2mol/L?min��
��4�������С��Ӧ������������¶Ȳ��䣩��ʹѹǿ����ƽ�������ʵ�Ũ������Ӧǰ�������������ƽ�ⲻ�䣬C�������������䣬����������������䣬�ܶȲ��䣬ƽ��Ħ������=
����Ӧǰ�����ʵ������䣬�����������䣬���Ի�������ƽ����Է���������
�ʴ�Ϊ�������䣬�����䣻
3A��g��+B��g��?2C��g��+2D��g��
��ʼ����mol�� 2 2 0 0
�仯����mol 1.2 0.4 0.8 0.8
ƽ������mol�� 0.8 1.6 0.8 0.8
��1��B��ƽ��Ũ��=
| n |
| V |
| 1.6mol |
| 2L |
�ʴ�Ϊ��0.8mol/L��
��2��A��ת����=
| ������ |
| ��ʼ�� |
| 1.2mol |
| 2mol |
�ʴ�Ϊ��60%��
��3����C��ʾ��ƽ����Ӧ����=
| ��c |
| ��t |
| ||
| 2min |
�ʴ�Ϊ��0.2mol/L?min��
��4�������С��Ӧ������������¶Ȳ��䣩��ʹѹǿ����ƽ�������ʵ�Ũ������Ӧǰ�������������ƽ�ⲻ�䣬C�������������䣬����������������䣬�ܶȲ��䣬ƽ��Ħ������=
| ���� |
| ���ʵ��� |
�ʴ�Ϊ�������䣬�����䣻
���������⿼���˻�ѧƽ��ļ���Ӧ�ã���Ҫ�Ƿ������ʡ�ƽ��Ũ�ȡ�Ӱ��ƽ������ط����жϣ����ջ����ǹؼ�����Ŀ�ϼ�

��ϰ��ϵ�д�
 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д�
�����Ŀ
���н���ʵ����̻���ʵ�ķ�Ӧ����ʽ����ȷ���ǣ�������
| A�������ռ�ʱ������ʹ����ͨʯӢ������SiO2+2NaOH�TNa2SiO3+H2O | ||||
| B���ں����ҵĽ���Һ������I-���еμ�H2O2�õ�I2��2I-+H2O2+2H+=I2+O2��+2H2O | ||||
C�����ȵ���˿��ˮ�Ӵ��������γɺ�ɫ�����㣺3Fe+4H2O��g��
| ||||
| D����84����Һ������Ч�ɷ�NaClO���͡�����顰����Ҫ�ɷ����ᣩ���ʹ�÷ų�������ClO-+Cl-+2H+=Cl2��+H2O |
��֪450��ʱ����ӦH2��g��+I2��g��?2HI��g����ƽ�ⳣ��K=100���ɴ��Ʋ���450��ʱ����ӦHI��g��?
H2��g��+
I2��g����ƽ�ⳣ��Ϊ��������
| 1 |
| 2 |
| 1 |
| 2 |
| A��0.01 | B��50 |
| C��100 | D��0.1 |
��ҩݭ�������к���һ��ɫ�أ����Ľṹ��ͼ����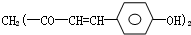 ���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������
���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������
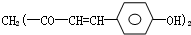 ���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������
���Ƴɵ���ֽ���Լ�������ԣ��ܹ���1mol�û�������Ӧ��NaOH��H2��������ֱ�Ϊ��������| A��3mol��3mol |
| B��1mol��5mol |
| C��6mol��8mol |
| D��2mol��10mol |
 ��ҵ����CO2��H2��һ�������������·�Ӧ�ϳɼ״����ų��������ȣ�CO2��g��+3H2��g��?CH3OH��g��+��H2O��g����H1 �ش��������⣮
��ҵ����CO2��H2��һ�������������·�Ӧ�ϳɼ״����ų��������ȣ�CO2��g��+3H2��g��?CH3OH��g��+��H2O��g����H1 �ش��������⣮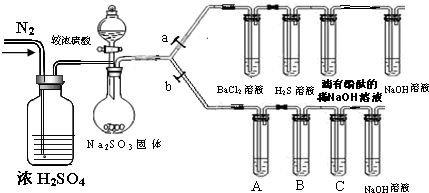
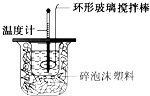 ijʵ��С����0.50mol?L-1 NaOH��Һ��0.55mol?L-1������Һ�����к��ȵIJⶨ��������0.50mol?L-1 NaOH��Һ
ijʵ��С����0.50mol?L-1 NaOH��Һ��0.55mol?L-1������Һ�����к��ȵIJⶨ��������0.50mol?L-1 NaOH��Һ