题目内容
(15分)新型材料纳米级铁粉与普通铁粉具有不同的性质。已知:在不同温度下,纳米级铁粉与水蒸气反应的固体产物不同,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。
(1)写出温度高于570℃时反应的化学方程式
。
(2)中学教材中用下图所示实验装置,完成铁粉与水蒸气反应的演示实验。实验中使用肥皂液的作用是 。
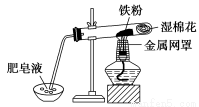
(3)如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精灯及其必要的仪器和物品,请在答题卷的方框中画出你设计的实验装置示意图(包括反应时容器中的物质)。
说明:①本题装置示意图中的仪器可以用下面的方式表示。
水槽: 试管:
试管: 蒸发皿:
蒸发皿: 玻璃导管:
玻璃导管: 或
或 (但应标示出在液面上或液面下)
(但应标示出在液面上或液面下)
②铁架台、石棉网、酒精灯、玻璃导管之间的联接胶管等,在示意图中不必画出。如需加热,在需加热的仪器下方,标以“△”表示。
(4)甲同学对实验后的黑色固体产物X含有哪些物质进行了如下实验:
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 取少量黑色固体产物X(假定成分分布均匀)放入试管中,加入盐酸,微热。 | 黑色粉末逐渐溶解,有少量气泡产生。 |
Ⅱ | 取实验Ⅰ反应后的溶液少许,滴加几滴KSCN溶液,振荡。 | 溶液没有出现血红色。 |
Ⅲ | 取实验Ⅰ反应后的溶液少许,滴加几滴酸性KMnO4溶液,振荡。 | 高锰酸钾溶液褪色。 |
根据以上实验事实,能确定固体X中存在的物质是 ,但不能确定X的成分,原因是 。
(5)乙同学为了探究实验后的固体产物是否存在Fe3O4设计下列实验方案:
①取固体样品m1 g,溶于足量的稀盐酸;
②向①反应后的溶液中加入足量H2O2的和氨水,充分反应后,过滤、洗涤、干燥;
③将②中所得固体进行灼烧,得到红棕色固体m2 g。
溶液X中发生氧化还原反应的离子方程式为 ;m1与m2的比值在 范围内时,才能确定固体样品中一定存在Fe3O4。
(15分)
(1)3Fe + 4H2O(g) Fe3O4 + 4H2(2分)
Fe3O4 + 4H2(2分)
(2)检验反应中生成的H2(2分)

(4)Fe(1分) 不能确定是否含有Fe3O4或FeO,(1分)如果混合物中存在Fe3O4,溶于盐酸生成的 Fe3+与 Fe反应会生成了 Fe2+;(1分)且溶液中的 Fe2+也有可能是 FeO与盐酸反应的产物(1分)
(5)2Fe2++2H++H2O2=2Fe3++2H2O(2分) 0.9< ≤0.97(2分)
≤0.97(2分)
【解析】
试题分析:(1)温度高于570℃时铁与水蒸气反应生成四氧化三铁和氢气,所以化学方程式为3Fe + 4H2O(g) Fe3O4 + 4H2;
Fe3O4 + 4H2;
(2)使用肥皂液的目的是检验生成的氢气,肥皂液产生气泡,说明有氢气生成;
(3)水蒸气的产生需要给盛放水的试管加热,水蒸气通入盛放铁粉的试管中,然后生成的氢气用另一导气管导出,用排水集气法收集,装置图如下: ;
;
(4)与盐酸反应产生气体,说明X中含有Fe;与KSCN溶液反应物红色出现,说明实验1后的溶液在无铁离子,但不能说明X中无四氧化三铁,因为即便X中含有四氧化三铁,溶于盐酸生成的 Fe3+与 Fe反应也会生成了 Fe2+;使高锰酸钾溶液褪色,说明实验1中的溶液中含有亚铁离子,但不能说明X中含有FeO,因为铁与盐酸反应也生成亚铁离子,所以不能确定是否含有Fe3O4或FeO;
(5)过氧化氢与亚铁离子反应生成铁离子和水,离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O;根据题意可知红棕色固体为氧化铁,若X全部是FeO,则m1与m2的关系利用铁元素守恒得:m1×56/72=m2×112/160,所以 =0.9,同理可得,若X全部是四氧化三铁,则m1×168/232=m2×112/160,
=0.9,同理可得,若X全部是四氧化三铁,则m1×168/232=m2×112/160,  =0.97,所以证明X中含有四氧化三铁的
=0.97,所以证明X中含有四氧化三铁的 的取值范围是0.9<
的取值范围是0.9< ≤0.97。
≤0.97。
考点:考查实验的设计,离子方程式的书写,反应的计算

 O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
O2+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO 、CO
、CO 。已知:
。已知: 表示阿伏加德罗常数,下列判断正确的是
表示阿伏加德罗常数,下列判断正确的是  中含有
中含有 个氧原子
个氧原子  中含有4
中含有4 个
个 的
的 溶解于1L水中,
溶解于1L水中, 的物质的量浓度为1 mol·L-1
的物质的量浓度为1 mol·L-1