题目内容
(10分)已知A、B、C、D四种短周期元素原子序数依次增大,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,B、C、D三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且X、Y、Z可两两相互反应生成盐和水,试推断并用相应的化学用语回答下列问题:
(1)D元素原子的结构示意图为_________________;
(2)X与C元素的最高价氧化物可以发生反应,该反应的离子方程式为___________________;
(3)A、B、C三种元素的原子半径由小到大的顺序为__________________________;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈___(填“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序为_____________________。
(1) (2)Al(OH)3+OH-=AlO2-+2H2O
(2)Al(OH)3+OH-=AlO2-+2H2O
(3)N<Al<Na (4)酸;c(OH-)<c(H+)<c(NH4+)<c(Cl-)
【解析】
试题分析:A、B、C、D四种短周期元素原子序数依次增大,D元素组成的单质在通常状况下呈黄绿色,所以D是Cl元素;B、C、D三种元素位于同一周期,B、C、D三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且X、Y、Z可两两相互反应生成盐和水,这说明一定含有氢氧化铝,因此为氢氧化钠与氢氧化铝反应,故B为Na元素、C为Al元素;A与D的原子序数之和等于B与C的原子序数之和,则A的原子序数为11+13-17=7,则A为氮元素。则
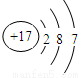
(1)Cl元素的原子序数是17,核外电子数为17,有3个电子层,各层电子数为2、8、7,原子结构示意图为 ;
;
(2)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
(3)同周期自左而右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,故原子半径N<Al<Na;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐是氯化铵。氯化铵溶液中,铵根离子水解,溶液呈酸性。由于水解程度弱,所以溶液中离子浓度由小到大的顺序为c(OH-)<c(H+)<c(NH4+)<c(Cl-)。
考点:考查元素周期表的结构以及元素周期律的应用

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
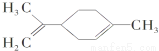
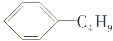 )互为同分异构体
)互为同分异构体
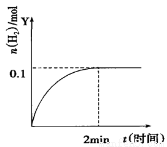
 H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是
H2(g)+I2(g) △H>0,H2的物质的量随时间的变化如图示,下列说法正确的是