题目内容
[化学一物质结构与性质〕
1、有E、Q、T、X、Z 五种前四周期元素,原子序数E<Q<T<<<Z。E、Q、T三种元素的基态原子具有相同的能级,且,I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状
态,且QT+ 2与ET2互为等电子体。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。
请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT+ 2的电子式 ,基态Z原子的核外电子排布式 ;
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有 等两种;
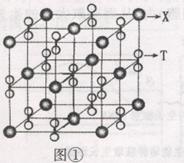
(3)化合物甲由T、X两种元素组成,其晶胞如图①,甲的化学式为 ;
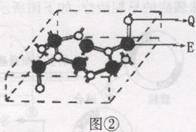
(4)化合物乙的晶胞如图②,乙由E、Q两种元素组成,硬度超过金刚石。
①乙的晶体类型为 ;
②乙的晶体中E、Q两种元素原子的杂化方式均为 。
答案:(1) ![]()
![]() (1分)
(1分)
(2)这两种氢化物均为极性分子、相互之间能形成氢键(2分)
(3)![]() (1分)
(1分)
(4)①原子晶体(1分) ②![]() (1分)
(1分)

 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案(13分)【化学一物质结构与性质】
A、B、M、X、Y、Z是元素周期表中的前20号元素.且原子序数依次增大。已知它们的部分化台物的性质如下表所示
| A的最简单氢化物 | B的最简单氢化物 | M的最简单氢化物 | X的氧化物 | Y的最简单氢化物 | Z的最高价氧化物 |
| 含氢量最高的有机物 | 水溶液呈碱性 | 水溶液呈酸性 | 两性氧化物 | 分子呈正四面体构型 | 对应水化物为最强酸 |
回答下列问题
(1)写出X原子的电子排布式 。
(2)A、B、M电负性由大到小的排列顺序为 。
(3)Y的最简单氢化物中,Y原子的杂化形式是 。
(4)B的最简单氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”)。
(5)比较熔点高低:A最高价氧化物的熔点 Y最高价氧化物的熔点。
(6)判断沸点高低:M氢化物的沸点 Z氢化物的沸点,原因是 。


 (2013?德州一模)【化学一物质结构与性质】
(2013?德州一模)【化学一物质结构与性质】