题目内容
20.下列有关物质的性质和该性质的应用均正确的是( )| A. | 铁具有良好的导电性,氯碱工业中可用铁作阳极电解食盐水 | |
| B. | 铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| C. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| D. | 氯化铝是一种电解质,可用于电解法制铝 |
分析 A.活性电极作阳极,电极反应溶液中的阴离子不反应;
B.活泼性强的金属作负极,被腐蚀;
C.Al(OH)3胶体能吸附水中的悬浮物,从而净水;
D.氯化铝是共价化合物,在熔融时不导电.
解答 解:A.活性电极作阳极,电极反应溶液中的阴离子不反应,所以氯碱工业中不能用铁作阳极电解食盐水,故A错误;
B.活泼性强的金属作负极,被腐蚀,铜的金属活泼性比铁的差,Fe、Cu形成原电池时,Fe为负极被腐蚀,所以在海轮外壳上装若干铜块不能减缓其腐蚀,故B错误;
C.明矾在溶液中电离出铝离子,铝离子能水解生Al(OH)3胶体,Al(OH)3胶体能吸附水中的悬浮物,从而净水,故C正确;
D.氯化铝是共价化合物,在熔融时不导电,所以不能电解熔融的氯化铝,应该电解熔融的氧化铝,故D错误.
故选C.
点评 本题考查了电解原理的应用、金属的腐蚀与防护、胶体的性质等,题目难度不大,侧重于基础知识的考查,注意氯化铝是共价化合物在熔融时不导电.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.将铝条投到一溶液中产生氢气,则此溶液中一定能够大量共存的离子组是( )
| A. | Cu2+、Cl-、NO3-、K+ | B. | HCO3-、K+、SO4 2-、Cl- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | Ba2+、Cl-、K+、SO4 2- |
8.能鉴别NH4Cl、K2SO4、(NH4)2SO4、NaCl 四瓶无色溶液的试剂是( )
| A. | Ba(NO3)2 溶液 | B. | AgNO3 溶液 | C. | Ba(OH)2 溶液 | D. | NaOH 溶液 |
15.金属钛易于和肌肉长在一起,可用于制造各种人造关节,因此被称为“生物金属”.工业上由钛铁矿(主要成分为FeTiO3,含少量Fe2O3)制备钛的工艺流程如下:
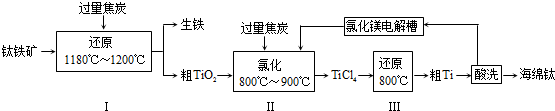
(1)进行步骤Ⅰ前,钛铁矿需要先粉碎成细颗粒,目的为增大反应速率.
(2)步骤Ⅰ中所发生的主要反应的化学方程式为FeTiO3+C$\frac{\underline{\;1180℃-1200℃\;}}{\;}$Fe+TiO2+CO↑.
(3)将步骤Ⅱ中所发生的主要反应记为反应①,则①的化学方程式为TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;有同学认为步骤Ⅱ中的物质转化中只需通入氯气,而无需加入焦炭就能实现,即发生反应②:TiO2+2Cl2 $\frac{\underline{\;高温\;}}{\;}$ TiCl4+O2.已知相关数据如下:
结合上表数据,从反应进行的方向角度分析加入焦炭的必要性加入焦炭后发生反应①,与反应②相比,△H减小,△S增大,更有利于反应在较低温度下向右进行.
(4)步骤Ⅲ中,反应物TiCl4应避免接触水,原因为防止TiCl4水解;反应结束后,用盐酸洗涤粗Ti,除去Mg、MgCl2(填化学式),即可制得海绵钛.

(1)进行步骤Ⅰ前,钛铁矿需要先粉碎成细颗粒,目的为增大反应速率.
(2)步骤Ⅰ中所发生的主要反应的化学方程式为FeTiO3+C$\frac{\underline{\;1180℃-1200℃\;}}{\;}$Fe+TiO2+CO↑.
(3)将步骤Ⅱ中所发生的主要反应记为反应①,则①的化学方程式为TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO;有同学认为步骤Ⅱ中的物质转化中只需通入氯气,而无需加入焦炭就能实现,即发生反应②:TiO2+2Cl2 $\frac{\underline{\;高温\;}}{\;}$ TiCl4+O2.已知相关数据如下:
| 反应 | △H/kJ•mol-1 | △S/J•K-1•mol-1 |
| ① | -72.1 | +220 |
| ② | +149 | +41 |
(4)步骤Ⅲ中,反应物TiCl4应避免接触水,原因为防止TiCl4水解;反应结束后,用盐酸洗涤粗Ti,除去Mg、MgCl2(填化学式),即可制得海绵钛.
12.在PCl5(g)?PCl3(g)+Cl2(g),达到平衡后,其它条件不变,向平衡体系中加入37Cl2,达到新平衡后,含37Cl的物质的量有( )
| A. | 只有PCl5 | B. | 只有PCl3 | ||
| C. | 只有Cl2 | D. | 以上三种物质都有 |
9.近年来科学家制造出大量的新物质,对下列三种物质的相关说法错误的是( )
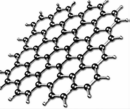 | 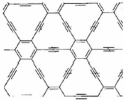 |  |
| 石墨烯:从石墨中分离出来,是最薄、最坚硬的物质 | 石墨块:平面网状结构的全碳分子,具有优良的化学稳定性 | 纳米碳管:具有优良的场发射性能,制作阴极显像管、储氢材料 |
| A. | 石墨烯具有良好的导电性 | |
| B. | 上述三种物质与金刚石互为同素异形体 | |
| C. | 石墨炔孔径略大于H2分子的直径,可作H2的提纯薄膜 | |
| D. | 上述三种物质与浓硫酸都能发生反应,但反应产物不同 |
10.铁有多种价态,将14.4g草酸亚铁(FeC2O4)与空气隔绝加热分解,最终得到7.2g铁的氧化物,则该铁的氧化物是( )
| A. | Fe3O4 | B. | Fe2O3 | C. | FeO | D. | FeO和Fe3O4 |
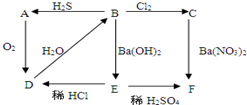 图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀.
图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀.