题目内容
下列说法正确的是( )
| A、实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B、用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度 |
| C、石油的分馏是物理变化,而煤的干馏是化学变化 |
| D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
考点:海水资源及其综合利用,石油的分馏产品和用途,乙醇的化学性质,氨基酸、蛋白质的结构和性质特点
专题:有机反应
分析:A、海带中的碘元素是以化合态存在,可以先将海带烧成灰,加水溶解,用氧化剂将碘离子氧化得到碘单质,最后用萃取分液法的到碘单质即可;
B、水浴加热的温度范围是25℃~100℃,实验室制取乙烯的温度是170℃;
C、根据石油的分馏和煤的干馏的概念来回答;
D、重金属盐可以使蛋白质变性.
B、水浴加热的温度范围是25℃~100℃,实验室制取乙烯的温度是170℃;
C、根据石油的分馏和煤的干馏的概念来回答;
D、重金属盐可以使蛋白质变性.
解答:
解:A、海带中的碘元素是以化合态存在,可以先将海带烧成灰,加水溶解,用氧化剂氯气将碘离子氧化得到碘单质,向溶液中加入四氯化碳萃取其中的碘单质,得到碘单质和四氯化碳的混合物,再用蒸馏法可以获取碘,取样→灼烧→溶解→过滤→加氧化剂氯气→萃取,故A错误;
B、水浴加热的控制的温度范围是25℃~100℃,但是实验室制取乙烯的温度是170℃,不能用水浴加热,故B错误;
C、石油的分馏是根据物质的沸点来实现物质的分离的方法,属于物理变化,而煤的干馏是将煤隔绝空气加强热使之分解的过程,属于化学变化,故C正确;
D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,前者使蛋白质盐析,后者使蛋白质变性,故D错误.
故选C.
B、水浴加热的控制的温度范围是25℃~100℃,但是实验室制取乙烯的温度是170℃,不能用水浴加热,故B错误;
C、石油的分馏是根据物质的沸点来实现物质的分离的方法,属于物理变化,而煤的干馏是将煤隔绝空气加强热使之分解的过程,属于化学变化,故C正确;
D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,前者使蛋白质盐析,后者使蛋白质变性,故D错误.
故选C.
点评:本题综合考查学生海带中提取碘单质的步骤、水浴加热的温度范围、分馏和干馏的概念以及蛋白质的性质等知识,属于综合知识的考查,难度大.

练习册系列答案
相关题目
在含0.3mol AlCl3的氯化铝溶液中加入200mL烧碱溶液,能生成0.1mol沉淀,则加入烧碱溶液物质的量浓度可能是( )
①1.5mol?L-1 ②4.5mol?L-1 ③5.5mol?L-1.
①1.5mol?L-1 ②4.5mol?L-1 ③5.5mol?L-1.
| A、② | B、① | C、③ | D、①、③ |
NA表示阿伏伽德罗常数,下列判断正确的是( )
A、16g CH4与18 g NH
| ||
| B、7.8gNa2O2与足量的CO2反应时转移的电子数为0.1NA | ||
| C、1 mol Cl2参加反应转移电子数一定为2 NA | ||
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol?L-1 |
X、Y、Z是三种气态物质,在一定温度下其变化符合如图.下列说法不正确的是( )
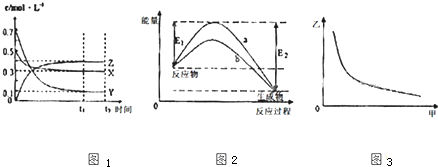

| A、该反应的化学方程式为X(g)+3Y(g)?2Z(g) |
| B、若图Ⅲ中甲表示压强,乙表示Z的含量,则其变化符合图Ⅲ中曲线 |
| C、该温度下,反应的平衡常数数值约为533.若升高温度,该反应的平衡常数减小,Y的转化率降低 |
| D、图II中曲线a、b可表示使用不同催化剂的能量变化曲线 |
X、Y、Z是短周期的三种主族元素,在周期表中的位置如图所示,下列说法正确的是( )
| X | |
| Y | Z |
| A、X的气态氢化物热稳定性强于Z的气态氢化物 |
| B、原子半径:X<Y<Z |
| C、若Y的最高正价为+m,则X,Z的最高正价一定为+(m+1) |
| D、Y和Z的最高价氧化物对应水化物酸性Y>Z |
下列化常用语中,正确的是( )
| A、两个氧分子-O2 |
| B、氢氧化铁的化学式-Fe(OH)3 |
| C、CO2中氧元素的化合价为+2价 |
| D、水通电得到氧气的化学方程式是2H2O=O2↑+2H2↑ |
氢硫酸在空气中有如此反应:2H2S+O2═2S↓+2H2O,下列不正确的是( )
| A、属于置换反应 |
| B、还原性:H2O>H2S |
| C、氧化性:O2>S |
| D、酸性:H2S>H2O |