题目内容
13.FeCl3是常用的化学试剂,请回答相关问题:(1)溶液呈黄色,是C引起的.
A、H2O B、Cl-
C、Fe3+ D、Fe(OH)3
(2)饱和FeCl3溶液滴入沸水中,片刻后冷至室温,再用光照时有光亮通路,说明形成的是B.
A、溶液 B、胶体 C、浊液
(3)检验Fe3+离子,常用下列哪种试剂A.
A、KSCN溶液 B、Cl2水 C、FeCl2溶液.
分析 (1)铁离子为黄色;
(2)用光照时有光亮通路,为丁达尔现象;
(3)铁离子遇KSCN溶液为血红色.
解答 解:(1)铁离子为黄色,则溶液呈黄色,是C引起的,故答案为:C;
(2)用光照时有光亮通路,为丁达尔现象,则为胶体分散系,故答案为:B;
(3)铁离子遇KSCN溶液为血红色,可检验铁离子,B、C均不能,故答案为:A.
点评 本题考查金属及化合物的性质,为高频考点,侧重于学生的分析应用能力的考查,注意把握物质的性质以及离子检验方法,题目难度不大.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
1.下列与化学有关的说法不正确的是( )
| A. | 洁厕灵的主要成分是盐酸,不能与“84”消毒液(主要成分是NaClO)混用 | |
| B. | 晶体的风化、煤的液化、石油的裂化都是化学变化 | |
| C. | 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
5.下列叙述正确的是( )
| A. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| B. | 钢铁吸氧腐蚀时,负极反应式为2H2O+O2+4e-═4OH- | |
| C. | 向醋酸钠溶液中加入适量醋酸至混合液pH=7时,溶液中c(Na+)=c(CH3COO-) | |
| D. | 0.1 mol/L NH4Cl溶液中,c(NH${\;}_{4}^{+}$)+c(H+)=c(Cl-) |
2.在足量的CuSO4溶液中加入下列试剂后,溶液质量减少了8g,则加入的物质是( )
| A. | 23g金属钠 | B. | 1mol/L BaCl2溶液100mL | ||
| C. | 56g金属铁 | D. | 20% NaOH溶液50g |
3.某气体通入品红溶液中,溶液褪色,加热后又恢复为原来的颜色.该气体是( )
| A. | SO2 | B. | O2 | C. | Cl2 | D. | CO2 |
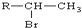 (R为烃基)
(R为烃基) .
. 某同学用如图所示装置探究SO2的性质及其有关实验.
某同学用如图所示装置探究SO2的性质及其有关实验.