题目内容
已知H2A在水中存在以下平衡:H2A?H++HA-,HA?H++A2-.回答以下问题:
(1)NaHA溶液 (填“显酸性”、“显碱性”、“显中性”或“酸碱性无法确定”,下同),某二元酸H2B电离方程式是:H2B═H++HB-,HB-?B2-+H+,NaHB溶液 .
(2)某温度下,向0.1mol/L的NaHA溶液中滴入0.1mol/LKOH溶液至中性,此时溶液中以下关系一定正确的是 (填字母).
A.c(H+)?c(OH-)═1×10-14 mol2/L2 B.c(Na+)+c(K+)═c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)═0.05mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)?Ca2+(aq)+A2-(aq)△H>0.
①温度升高时,Ksp (填“增大”、“减小”或“不变”,下同).
②滴加少量浓盐酸,c(Ca2+) ,原因是 (用文字和离子方程式说明).
(1)NaHA溶液
(2)某温度下,向0.1mol/L的NaHA溶液中滴入0.1mol/LKOH溶液至中性,此时溶液中以下关系一定正确的是
A.c(H+)?c(OH-)═1×10-14 mol2/L2 B.c(Na+)+c(K+)═c(HA-)+2c(A2-)
C.c(Na+)>c(K+) D.c(Na+)+c(K+)═0.05mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s)?Ca2+(aq)+A2-(aq)△H>0.
①温度升高时,Ksp
②滴加少量浓盐酸,c(Ca2+)
考点:弱电解质在水溶液中的电离平衡,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)根据HA-的电离溶液呈酸性,HA-的水解溶液呈碱性,但不能确定HA-的电离程度和水解程度的大小;HB-能电离但不水解,根据氢离子和氢氧根离子浓度相对大小确定溶液的酸碱性;
(2)A、水的离子积常数与温度有关,温度越高,水的离子积常数越大;
B、根据溶液中电荷守恒判断;
C、根据题意知NaHA溶液呈酸性,Na2A溶液呈碱性,则向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量;
D、根据题意知NaHA溶液呈酸性,Na2A溶液呈碱性,则向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的体积应大于KOH的体积,据此确定钠离子和钾离子浓度之和;
(3)①该反应为吸热反应,温度升高,平衡正向移动,然后判断Ksp;
②加盐酸,促进难溶盐的电离,使平衡向正反应方向移动.
(2)A、水的离子积常数与温度有关,温度越高,水的离子积常数越大;
B、根据溶液中电荷守恒判断;
C、根据题意知NaHA溶液呈酸性,Na2A溶液呈碱性,则向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量;
D、根据题意知NaHA溶液呈酸性,Na2A溶液呈碱性,则向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的体积应大于KOH的体积,据此确定钠离子和钾离子浓度之和;
(3)①该反应为吸热反应,温度升高,平衡正向移动,然后判断Ksp;
②加盐酸,促进难溶盐的电离,使平衡向正反应方向移动.
解答:
解:(1)HA-的电离溶液呈酸性,HA-的水解溶液呈碱性,但不能确定HA-的电离程度和水解程度的大小,所以酸碱性无法确定;HB-能电离但不水解,导致溶液中c(H+)>c(OH-),所以溶液呈酸性;
故答案为:酸碱性无法确定;酸性;
(2)A、水的离子积常数与温度有关,温度越高,水的离子积常数越大,温度未知,所以水的离子积常数也未知,故A错误;
B、溶液呈电中性,溶液中阴阳离子所带电荷相等,溶液呈中性,氢离子浓度等于氢氧根离子浓度,所以c(Na+)+c(K+)=c(HA-)+2c(A2-),故B正确;
C、NaHA溶液呈酸性,Na2A溶液呈碱性,向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量,所以同一混合溶液中c(Na+)>c(K+),故C正确;
D、NaHA溶液呈酸性,Na2A溶液呈碱性,向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的体积应大于氢氧化钾的体积,所以c(Na+)+c(K+)>0.05mol/L,故D错误;
故答案为:BC;
(3)①该反应为吸热反应,温度升高,平衡正向移动,Ksp增大,故答案为:增大;
②加盐酸发生反应:A2-+H+?HA-,A2-浓度减小,CaA的溶解平衡向右移动,n(Ca2+)显著增大,而溶液体积变化不大,所以c(Ca2+)增大,
故答案为:增大;加盐酸发生反应:A2-+H+?HA-,A2-浓度减小,CaA的溶解平衡向右移动,n(Ca2+)显著增大,而溶液体积变化不大,所以c(Ca2+)增大.
故答案为:酸碱性无法确定;酸性;
(2)A、水的离子积常数与温度有关,温度越高,水的离子积常数越大,温度未知,所以水的离子积常数也未知,故A错误;
B、溶液呈电中性,溶液中阴阳离子所带电荷相等,溶液呈中性,氢离子浓度等于氢氧根离子浓度,所以c(Na+)+c(K+)=c(HA-)+2c(A2-),故B正确;
C、NaHA溶液呈酸性,Na2A溶液呈碱性,向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的物质的量应大于氢氧化钾的物质的量,所以同一混合溶液中c(Na+)>c(K+),故C正确;
D、NaHA溶液呈酸性,Na2A溶液呈碱性,向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性时,NaHA的体积应大于氢氧化钾的体积,所以c(Na+)+c(K+)>0.05mol/L,故D错误;
故答案为:BC;
(3)①该反应为吸热反应,温度升高,平衡正向移动,Ksp增大,故答案为:增大;
②加盐酸发生反应:A2-+H+?HA-,A2-浓度减小,CaA的溶解平衡向右移动,n(Ca2+)显著增大,而溶液体积变化不大,所以c(Ca2+)增大,
故答案为:增大;加盐酸发生反应:A2-+H+?HA-,A2-浓度减小,CaA的溶解平衡向右移动,n(Ca2+)显著增大,而溶液体积变化不大,所以c(Ca2+)增大.
点评:本题考查了盐溶液酸碱性的判断、溶液中离子浓度的关系、外界条件对化学平衡的影响等知识点,难度较大,根据温度、电解质溶液对难溶物性质的影响和电荷守恒、物料守恒来分析解答即可.

练习册系列答案
相关题目
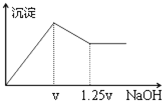 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl?)与c(SO42?)之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的关系如图所示,则溶液中c(Cl?)与c(SO42?)之比为( )| A、1:1 | B、2:3 |
| C、3:2 | D、2:1 |
生活中处处有化学.下列说法正确的是( )
| A、煎炸食物的花生油和牛油都是可皂化的饱和酯类 |
| B、做衣服的棉和麻均与淀粉互为同分异构体 |
| C、制饭勺、饭盒、高压锅等的不锈钢是合金 |
| D、磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
关于下列实验装置的叙述中,正确的是( )
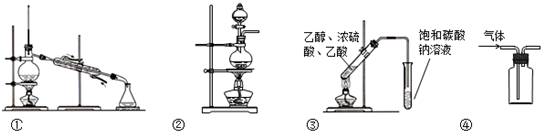

| A、装置①常用于分离互不相溶的液体 |
| B、装置②可用于实验室加热酒精与浓硫酸的混合物制取乙烯 |
| C、装置③可用于制备乙酸乙酯 |
| D、装置④可用于收集NO、CO2等气体 |
在用0.1000mol/LNaOH溶液测定食醋总酸含量的实验中,下列说法正确的是( )
| A、碱式滴定管没有润洗会使测定含量偏低 |
| B、用移液管移取一定体积食醋时,应将移液管垂直放入稍倾斜的容器中,并将尖嘴贴紧容器 |
| C、该实验应用甲基橙作指示剂 |
| D、如果氢氧化钠溶液滴加过量,只能重新实验 |
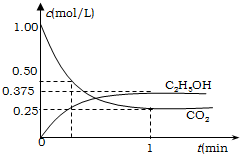 前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的重大问题.
前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的重大问题.