题目内容
 工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.
工业上以黄铜矿(主要成分CuFeS2)为原料制备金属铜,有如下两种工艺.I.火法熔炼工艺:将处理过的黄铜矿加人石英,再通人空气进行焙烧,即可制得粗铜.
(1)焙烧的总反应式可表示为2CuFeS2+2SiO2+5O2═2Cu+2FeSi03+4SO2该反应的氧化剂是
(2)下列处理SO2的方法,不合理的是
A.高空排放 B.用纯碱溶液吸收制备亚硫酸钠
C.用氨水吸收后,再经氧化制备硫酸铵 D.用BaCl2溶液吸收制备BaSO3
(3)炉渣主要成分有FeO、Fe2O3、SiO2,Al2O3等,为得到Fe2O3加盐酸溶解后,后续处理过程中,未涉及到的操作有
A.过滤 B.加过量NaOH溶液 C.蒸发结晶 D.灼烧 E.加氧化剂
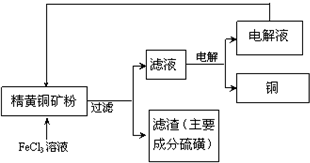
Ⅱ.FeCl3溶液浸取工艺:其生产流程如图所示.
(4)浸出过程中,CuFeS2与FeCl3溶液反应的离子方程式为
(5)该工艺流程中,可以循环利用的物质是
(6)若用石墨电极电解滤液,写出阳极的电极反式
(7)黄铜矿中含少量Pb,调节Cl-浓度可控制滤液中Pb2+的浓度,当c(Cl-)=2mol?L-1,时溶液中Pb2+物质的量浓度为
考点:制备实验方案的设计,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题,元素及其化合物
分析:(1)根据反应中元素化合价降低的为氧化剂判断;
(2)SO2属于有毒气体,与BaCl2溶液不反应;
(3)炉渣主要成分有FeO、Fe2O3、SiO2,Al2O3等加过量HCl溶液溶解,过滤得到滤液为Fe2+、Fe3+、Al3+,加氢氧化钠,过滤,把滤渣灼烧得Fe2O3;
(4)CuFeS2与FeCl3溶液反应,-2价的S元素被三价铁离子氧化为S;
(5)CuFeS2与FeCl3溶液反应生成FeCl2、CuCl2溶液,电解该溶液得到Cu和Fe3+;
(6)石墨电极电解滤液,阳极上失电子发生氧化反应;
(7)已知氯离子的浓度,结合Ksp计算Pb2+物质的量浓度.
(2)SO2属于有毒气体,与BaCl2溶液不反应;
(3)炉渣主要成分有FeO、Fe2O3、SiO2,Al2O3等加过量HCl溶液溶解,过滤得到滤液为Fe2+、Fe3+、Al3+,加氢氧化钠,过滤,把滤渣灼烧得Fe2O3;
(4)CuFeS2与FeCl3溶液反应,-2价的S元素被三价铁离子氧化为S;
(5)CuFeS2与FeCl3溶液反应生成FeCl2、CuCl2溶液,电解该溶液得到Cu和Fe3+;
(6)石墨电极电解滤液,阳极上失电子发生氧化反应;
(7)已知氯离子的浓度,结合Ksp计算Pb2+物质的量浓度.
解答:
解:(1)焙烧的总反应式可表示为2CuFeS2+2SiO2+5O2═2Cu+2FeSi03+4SO2该反应中化合价发生降低有CuFeS2中的Cu元素、O2中的O元素,所以氧化剂为CuFeS2、O2,故答案为:CuFeS2、O2;
(2)A.SO2属于有毒气体,高空排放会污染大气,故A错误;
B.SO2与碳酸钠溶液反应生成亚硫酸钠,则可以用纯碱溶液吸收制备亚硫酸钠,故B正确;
C.用氨水吸收后二氧化硫得到亚硫酸铵,再经氧化制备硫酸铵,故C正确;
D.二氧化硫与BaCl2溶液不反应,所以不能用BaCl2溶液吸收二氧化硫,也得不到BaSO3,故D正确;
故答案为:A、D;
(3)炉渣主要成分有FeO、Fe2O3、SiO2,Al2O3等加过量HCl溶液溶解,过滤得到滤液为Fe2+、Fe3+、Al3+,加过量氢氧化钠,过滤得到的滤渣为氢氧化铁沉淀和氢氧化亚铁沉淀,把滤渣灼烧得Fe2O3;则过程中涉及的操作为ABD、未涉及的操作为CE;
故答案为:C、E;
(4)CuFeS2与FeCl3溶液反应,-2价的S元素被三价铁离子氧化为S,同时生成生成FeCl2、CuCl2,则反应的离子方程式为:CuFeS2+4Fe3+=Cu2++5Fe2++S;
故答案为:CuFeS2+4Fe3+=Cu2++5Fe2++S;
(5)CuFeS2与FeCl3溶液反应生成FeCl2、CuCl2溶液,电解该溶液得到Cu和Fe3+,则电解时反应生成FeCl3,所以可以循环利用的物质是FeCl3;
故答案为:FeCl3;
(6)石墨电极电解滤液,阳极上失电子发生氧化反应,由于失电子能力亚铁离子大于氯离子,所以在阳极上亚铁离子失电子生成铁离子,则电极反应式为:Fe2+-e-=Fe3+,故答案为:Fe2+-e-=Fe3+;
(7)已知氯离子的浓度c(Cl-)=2mol?L-1,KSP(PbCl2)=1×10-5=c(Pb2+)×c2(Cl-),则Pb2+物质的量浓度c(Pb2+)=
=2.5×10-6mol?L-1;
故答案为:2.5×10-6.
(2)A.SO2属于有毒气体,高空排放会污染大气,故A错误;
B.SO2与碳酸钠溶液反应生成亚硫酸钠,则可以用纯碱溶液吸收制备亚硫酸钠,故B正确;
C.用氨水吸收后二氧化硫得到亚硫酸铵,再经氧化制备硫酸铵,故C正确;
D.二氧化硫与BaCl2溶液不反应,所以不能用BaCl2溶液吸收二氧化硫,也得不到BaSO3,故D正确;
故答案为:A、D;
(3)炉渣主要成分有FeO、Fe2O3、SiO2,Al2O3等加过量HCl溶液溶解,过滤得到滤液为Fe2+、Fe3+、Al3+,加过量氢氧化钠,过滤得到的滤渣为氢氧化铁沉淀和氢氧化亚铁沉淀,把滤渣灼烧得Fe2O3;则过程中涉及的操作为ABD、未涉及的操作为CE;
故答案为:C、E;
(4)CuFeS2与FeCl3溶液反应,-2价的S元素被三价铁离子氧化为S,同时生成生成FeCl2、CuCl2,则反应的离子方程式为:CuFeS2+4Fe3+=Cu2++5Fe2++S;
故答案为:CuFeS2+4Fe3+=Cu2++5Fe2++S;
(5)CuFeS2与FeCl3溶液反应生成FeCl2、CuCl2溶液,电解该溶液得到Cu和Fe3+,则电解时反应生成FeCl3,所以可以循环利用的物质是FeCl3;
故答案为:FeCl3;
(6)石墨电极电解滤液,阳极上失电子发生氧化反应,由于失电子能力亚铁离子大于氯离子,所以在阳极上亚铁离子失电子生成铁离子,则电极反应式为:Fe2+-e-=Fe3+,故答案为:Fe2+-e-=Fe3+;
(7)已知氯离子的浓度c(Cl-)=2mol?L-1,KSP(PbCl2)=1×10-5=c(Pb2+)×c2(Cl-),则Pb2+物质的量浓度c(Pb2+)=
| 1×10-5 |
| (2)2 |
故答案为:2.5×10-6.
点评:本题考查了物质的制备方案设计,题目涉及氧化还原反应、元素化合物性质、实验方案设计、电解原理的应用、溶度积的有关计算等,侧重对化学基本操作与技能的考查,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度中等.

练习册系列答案
相关题目
将CO2和C加入密闭容器中,在一定条件下发生反应:CO2(g)+C(s)?2CO(g),忽略固体体积,平衡时CO的体积分数(%)随温度和压强的变化如下表所示:
下列判断不正确的是( )
| 温度/℃ CO的体积分数/% 压强/MPa | 1.0 | 2.0 | 3.0 |
| 800 | 54.0 | a | b |
| 900 | c | 75.0 | d |
| 1000 | e | f | 80.0 |
| A、b<f |
| B、900℃,2.0MPa的转化率为60% |
| C、K(1000℃)=3.2 |
| D、K(1000℃)>K(800℃) |
在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A、由水电离的c(H+)=l×l0-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
| C、Kw/c(H+)=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- |
| D、FeCl2溶液:K+、Na+、SO42-、AlO2- |
把250ml含有BaCl2和AlCl3的混合溶液分成5等份,取一份加入含a mol Na2SO4的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol AgNO3的溶液,恰好使氯离子完全沉淀,则该混合溶液中铝离子浓度约为( )
A、
| ||
B、
| ||
C、
| ||
| D、4(b-2a)mol/L |
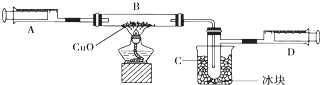
 Na2O2与水的反应实际可以分解为两个阶段:Na2O2+2H2O=2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2=2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:
Na2O2与水的反应实际可以分解为两个阶段:Na2O2+2H2O=2NaOH+H2O2,反应放热,反应放出的热量使部分H2O2受热分解:2H2O2=2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验: