题目内容
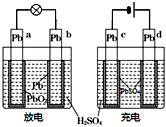 已知蓄电池在充电时作电解池,放电时作原电池.如图是铅蓄电池的工作示意图,其反应原理为:PbO2+Pb+2H2SO4
已知蓄电池在充电时作电解池,放电时作原电池.如图是铅蓄电池的工作示意图,其反应原理为:PbO2+Pb+2H2SO4| 放电 |
| 充电 |
| A、b电极放电后转化为c电极 |
| B、电极a和d都发生还原反应 |
| C、b的电极反应式:Pb+SO42--2e→PbSO4 |
| D、放电后硫酸溶液的pH增大 |
考点:原电池和电解池的工作原理
专题:
分析:左池为放电时状态,a为正极b为负极,负极反应式为:Pb+SO42--2e-=PbSO4,正极反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,右池为充电时状态,c为阴极,d为阳极,电池充电时,阳极上的反应是放电时的正极反应的逆过程,阴极上的反应是放电时负极反应的逆过程,据此分析.
解答:
解:A、放电时的负极充电时为阴极,故A正确;
B、a即发生还原反应,d极发生氧化反应,故B错误;
C、b为负极,负极反应式为:Pb+SO42--2e-=PbSO4,故C正确;
D、放电时消耗硫酸,氢离子浓度降低,溶液pH增大,故D正确;
故选B.
B、a即发生还原反应,d极发生氧化反应,故B错误;
C、b为负极,负极反应式为:Pb+SO42--2e-=PbSO4,故C正确;
D、放电时消耗硫酸,氢离子浓度降低,溶液pH增大,故D正确;
故选B.
点评:本题考查铅蓄电池,注意原电池和电解池的分析,明确工作原理及电子守恒是解答本题的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
0.03molCu投入到一定量的浓HNO3 中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2 的体积为( )
| A、504mL |
| B、336mL |
| C、224mL |
| D、168mL |
下列离子方程式书写正确的是( )
| A、实验室用大理石和稀盐酸制取二氧化碳:2H++CO32-=CO2↑+H2O |
| B、少量的SO2气体通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C、向AlCl3溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
| D、NaHCO3溶液与NaAlO2溶液混合:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32- |
下列有机物命名正确的是( )
A、 2-乙基丙烷 2-乙基丙烷 |
B、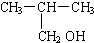 2-甲基丙醇 2-甲基丙醇 |
C、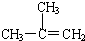 2-甲基丙烯 2-甲基丙烯 |
D、 2,2-二甲基-3-丁醇 2,2-二甲基-3-丁醇 |
某同学为检验溶液中是否含有常见的几种离子,进行了如图所示的实验操作.其中,检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是( )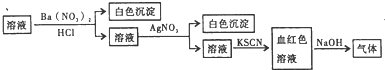

| A、原溶液中一定含有SO42- |
| B、原溶液中不一定含有NH4+ |
| C、原溶液中一定含有Cl- |
| D、原溶液中含Fe2+、Fe3+至少有一种 |
对于常温下pH为2的盐酸,叙述不正确的是( )
| A、c(H+)=c(Cl-)+c(OH-) |
| B、与等体积pH=12的氨水混合后所得溶液显碱性 |
| C、由H2O电离出的c(H+)=1.0×10-12 mol?L-1 |
| D、与等体积0.01 mol?L-1醋酸钠溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |
下列有关电子云和原子轨道的说法正确的是( )
| A、原子核外的电子象云雾一样笼罩在原子核周围,故称电子云 |
| B、s亚层的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 |
| C、p亚层的原子轨道呈纺锤形,随着电子层数的增加,p亚层原子轨道也在增多 |
| D、s、p电子原子轨道的平均半径随电子层的增大而增大 |
下列各组实验需水浴加热的是( )
①实验室制乙烯 ②制乙酸乙酯 ③制硝基苯 ④制酚醛树酯 ⑤银镜反应 ⑥制溴苯.
①实验室制乙烯 ②制乙酸乙酯 ③制硝基苯 ④制酚醛树酯 ⑤银镜反应 ⑥制溴苯.
| A、①②③④ | B、②③⑤ |
| C、③④⑤ | D、④⑤⑥ |