��Ŀ����
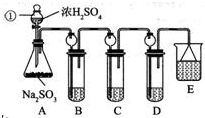
9�����������һ�ֵ��͵�ǿ�����������������գ�������KMnO4������Һ����Cu2S��CuS�Ļ����ʱ�������ķ�Ӧ���£�
��MnO4-+Cu2S+H+Cu2++SO2��+Mn2++H2O��δ��ƽ��
��MnO4-+CuS+H+Cu2++SO2��+Mn2++H2O��δ��ƽ��
��1�����й��ڷ�Ӧ�ٵ�˵���д������d������ĸ��ţ���
a����������Ԫ����Cu��S b���������뻹ԭ�������ʵ���֮��Ϊ8��5
c������2.24L������£�SO2��ת�Ƶ��ӵ����ʵ���0.8mol d����ԭ�Ե�ǿ����Mn2+��Cu2S
����ϡ�����У�KMnO4�� ��NH4��2Fe��SO4��2Ҳ�ܷ���������ԭ��Ӧ��
��2��д��KMnO4�루NH4��2Fe��SO4��2��Ӧ�����ӷ���ʽ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
��3��������480mL 0.1mol/L Fe2+��Һ�����ȡ��NH4��2Fe��SO4��2•6H2O��M=392g/mol��������Ϊ19.6g����Ҫ�IJ���������500mL����ƿ���ձ�����ͷ�ιܡ���������
��ʵ���ҿ������̿���Ҫ�ɷ�ΪMnO2���Ʊ�KMnO4���������£�������ʹ���̿������KOH��s����KClO3��s����Ӧ������K2MnO4������أ���KCl����ˮ�ܽ⣬��ȥ�������ữ��Һ��K2MnO4ת��ΪMnO2��KMnO4������ȥ����MnO2��Ũ���ᾧ�õ�KMnO4���壮��ش�
��4�������̿��Ʊ�K2MnO4�Ļ�ѧ����ʽ�ǣ�6KOH+KClO3+3MnO2�T3K2MnO4+KCl+3H2O��
��5��K2MnO4ת��ΪKMnO4�ķ�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1��2�����õ����ű�ʾ���ӵ�ת�����
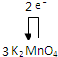 ��
��
���� I����1�����ݻ��ϼ۵ı仯�ж�������ԭ��Ӧ����ظ������������ԭ��Ӧ���������ͻ�ԭ��֮���ʧ���ӵ����ʵ�����ȼ���ת�Ƶ��ӵ����ʵ�������������ԭ��Ӧ�л�ԭ���Ļ�ԭ�Դ��ڻ�ԭ����Ļ�ԭ�ԣ�
��2����Ӧ��MnԪ�صĻ��ϼ۽��ͣ�FeԪ�صĻ��ϼ����ߣ�����������ԭ��Ӧ�����غ㡢����ա�ԭ���غ���ƽд�����ӷ���ʽ��
II����3��������480mL������û�иù�������ƿ��ʵ����Ҫ����500mL����Ҫ500mL����ƿ�����m=cVM���㣻
III����4����Ӧ��ΪKOH��KClO3��MnO2��������ΪK2MnO4������أ���KCl��ˮ�����������غ㶨����д��Ӧ����ʽ��
��5��K2MnO4ת��ΪKMnO4�ķ�Ӧ��K2MnO4��2KMnO4+MnO2��MnԪ�صĻ��ϼۼ������ֽ��ͣ����ݵ�ʧ�����غ���㣮
��� �⣺I����1��a����Ӧ��ͭԪ�ػ��ϼ۴�+1�����ߵ�+2�ۣ���Ԫ�ػ��ϼ۴�-2�����ߵ�+4�ۣ����ϼ����ߵ�Ԫ�ر����������Ա�������Ԫ����S��Cu����a��ȷ��
b����Ԫ�ػ��ϼ۽��ͣ���+7�۽���Ϊ+2�ۣ�Cu2SԪ�ػ��ϼ۶���������ԭ����1molMnO4-�õ�5mol���ӣ���Ӧ��ͭԪ�ػ��ϼ۴�+1�����ߵ�+2�ۣ���Ԫ�ػ��ϼ۴�-2�����ߵ�+4�ۣ�1molCu2Sʧȥ8mol���ӣ����������뻹ԭ�������ʵ���֮��Ϊ8��5����b��ȷ��
c������2.24LL������£�SO2ʱ�����ʵ���Ϊ0.1mol����Ӧ��Cu2S���ʵ���Ϊ0.1mol����Ӧ��ת�Ƶ��ӵ����ʵ����ǣ�
Cu+��Cu2+��e-�� S2-��SO2��6e-��
1 1 1 6
0.2mol 0.2mol 0.1mol 0.6mol
���Ե���ת�ƹ�0.8mol����c��ȷ��
d��������ԭ��Ӧ�л�ԭ���Ļ�ԭ�Դ��ڻ�ԭ����Ļ�ԭ�ԣ���ԭ�Ե�ǿ����ϵ�ǣ�Mn2+��Cu2S����d����
�ʴ�Ϊ��d��
��2����Ӧ��MnԪ�صĻ��ϼ۽��ͣ�FeԪ�صĻ��ϼ����ߣ����������Fe2+�ķ�Ӧ��MnO4-��Mn2+��5e-��Fe2+��Fe3+��e-�����ݵ����غ㣬�����Ӻ���������ǰ��5������ԭ���غ�͵���غ�õ���Ӧ�����ӷ���ʽΪ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
�ʴ�Ϊ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O��
II����3��������480mL������û�иù�������ƿ��ʵ����Ҫ����500mL������500mL 0.1mol/L Fe2+��Һ����Ҫ500mL����ƿ��m=cVM=0.5L��0.1mol/L��392g/mol=19.6g������Ҫ�IJ�������Ϊ�ձ� ��ͷ�ι� ��������
�ʴ�Ϊ��19.6��500mL����ƿ���ձ�����ͷ�ιܡ���������
III����4����Ӧ��ΪKOH��KClO3��MnO2��������ΪK2MnO4������أ���KCl��ˮ���÷�ӦΪ6KOH+KClO3+3MnO2�T3K2MnO4+KCl+3H2O��
�ʴ�Ϊ��6KOH+KClO3+3MnO2�T3K2MnO4+KCl+3H2O��
��5��K2MnO4ת��ΪKMnO4�ķ�Ӧ��K2MnO4=2KMnO4+MnO2��MnԪ�صĻ��ϼ���+6������Ϊ+7�ۣ�MnԪ�صĻ��ϼ���+6�۽���Ϊ+4�ۣ����������ͻ�ԭ�������ʵ���֮��Ϊ1��2����Ӧ��ת����2e-���õ����ű�ʾ���ӵ�ת�����Ϊ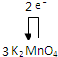 ��
��
�ʴ�Ϊ��1��2��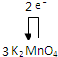 ��
��
���� ���⿼��������ԭ��Ӧ���㡢����ʽ����ƽ����Һ�����ƣ����շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ�������������ԭ��Ӧ���㼰ת�Ƶ��ӵĿ��飬ע��ӻ��ϼ۽Ƕȷ�������Ŀ�Ѷ��еȣ�

 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д�| A�� | ͭ����ϡ���Cu+4H++2NO3-�TCu2++2NO2��+2H2O | |
| B�� | ���Ȼ�����Һ��ʴӡˢ��·�壺2Fe3++3Cu�T2Fe+3Cu2+ | |
| C�� | С�մ���Һ�м���������ʯ��ˮ��HCO3-+Ca2++OH-�TCaCO3��+H2O | |
| D�� | ����������������Һ��Al+2OH-+H2O�TAlO2-+2H2�� |
| A�� | ��Կ��ȡ�������������̷�ĩ | |
| B�� | ��ȼ�ŵľƾ�����ֱ�����Ӿƾ� | |
| C�� | ʵ���Ҽ��ȸ��������������װ����ȡ���� | |
| D�� | ʵ���ҽ����������Ʊ�����ú���� |

| A�� | �û�����ķ���ʽΪC17H17N2O6 | |
| B�� | �û�����ķ����к������ֲ�ͬ�Ĺ����� | |
| C�� | �û�����IJ����Ͷ�Ϊ10 | |
| D�� | �û������ܷ���ˮ�ⷴӦ���ۺϷ�Ӧ��ȡ����Ӧ����ȥ��Ӧ |
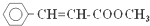 �������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫���й����������������У�����ȷ���ǣ�������
�������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫���й����������������У�����ȷ���ǣ�������| A�� | ����������Ȼ�̼��Һ�����ӳɷ�Ӧ | |
| B�� | ��ʹ���Ը��������Һ��ɫ | |
| C�� | �ڼ����������ܷ���ˮ�ⷴӦ | |
| D�� | �����ܷ����Ӿ۷�Ӧ |
| A�� | H++OH-�TH2O��H=-57.3kJ•mol-1 | |
| B�� | 2NaOH��aq��+H2SO4��aq���TNa2SO4��aq��+2H2O��l����H=-114.6kJ•mol-1 | |
| C�� | 2C8H18��l��+25O2��g���T16CO2��g��+18H2O��g����H=-11036kJ•mol-1 | |
| D�� | 2C8H18��l��+25O2��g���T16CO2��g��+18H2O��l����H=-5518kJ•mol-1 |
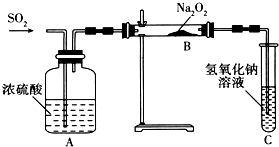
 ���ֶ���������Ԫ��A��B��C��D�����ڷǽ���Ԫ�أ����������ڱ��е�λ����ͼ��ʾ����ش������⣺
���ֶ���������Ԫ��A��B��C��D�����ڷǽ���Ԫ�أ����������ڱ��е�λ����ͼ��ʾ����ش������⣺