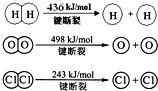
题目内容
实验证明:若用电解熔融KCl制钾,发现钾熔于熔融KCl中难分离,且电解过程中容易发生爆炸事故等.因而工业不用电解熔融KCl制钾,而用金属钠与KCl共熔置换制钾:
Na(l)+KCl(l)?NaCl(l)+K(g)△H>0. 下面是四种物质的熔沸点:
根据平衡移动原理,可推知用Na与KCl反应制取金属钾的适宜温度是( )
Na(l)+KCl(l)?NaCl(l)+K(g)△H>0. 下面是四种物质的熔沸点:
| K | Na | KCl | NaCl | |
| 熔点/℃ | 63.6 | 97.8 | 770 | 801 |
| 沸点/℃ | 774 | 882.9 | 1500 | 1413 |
| A、低于770℃ |
| B、约850℃? |
| C、高于882.9℃ |
| D、1413~1500℃? |
考点:金属冶炼的一般原理
专题:
分析:根据平衡移动原理,为使反应向正反应方向进行,可使生成物从平衡体系中分离出来,根据Na和K的沸点大小,制取的适宜温度应能使K蒸汽分离出,而钠为液体.
解答:
解:制取的适宜温度应能使K蒸汽分离出,而钠为液体,选择的温度应在774℃~882.9℃之间,则只有B符合.
故选B.
故选B.
点评:本题考查化学平衡知识,侧重于平衡移动的原理的应用,难度不大,注意从浓度对平衡移动的影响的角度分析.

练习册系列答案
相关题目
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
| A、甲的分子数比乙的分子数多 |
| B、甲的物质的量比乙的物质的量少 |
| C、甲的摩尔体积比乙的摩尔体积小 |
| D、甲的相对分子质量比乙的小 |
在常温下,不能与晶体硅发生化学反应的是( )
| A、氟气 | B、氢氟酸 |
| C、KOH溶液 | D、氧气 |
下列各种环境下的离子组合能够大量共存的是( )
| A、中性溶液中,Na+、Fe3+、SO42-、ClO- |
| B、pH=0的溶液中,Al3+、NH4+、Ca2+、SO42- |
| C、c(H+)=1.0×10-14mol?L-1的溶液中,Na+、AlO2-、S2-、SO32- |
| D、石蕊试纸变红的溶液中,Fe2+、I-、NO3-、ClO- |
下列有关物质结构的表述正确的是( )
| A、次氯酸的结构式:H-Cl-O | ||
B、中子数为20的氯原子:
| ||
C、四氯化碳的电子式: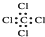 | ||
D、Cl-的结构示意图: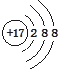 |