题目内容
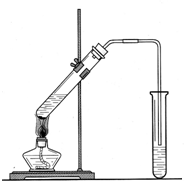
请回答下列实验问题
(1)实验室制取氨气时,采用 法收集气体.
(2)实验室制取氨气的发生装置,与初中学过的实验室制取 相同.
(3)干燥氨气通常使用 .
(4)检验氨气是否已经收集满,通常方法是 .
(1)实验室制取氨气时,采用
(2)实验室制取氨气的发生装置,与初中学过的实验室制取
(3)干燥氨气通常使用
(4)检验氨气是否已经收集满,通常方法是
考点:氨的制取和性质
专题:
分析:(1)氨气的密度比空气小;
(2)实验室制取氨气需要加热,与初中制取O2类似;
(3)氨气是碱性气体用碱性干燥剂干燥;
(4)依据氨气遇湿润的红色石蕊试纸变蓝证明.
(2)实验室制取氨气需要加热,与初中制取O2类似;
(3)氨气是碱性气体用碱性干燥剂干燥;
(4)依据氨气遇湿润的红色石蕊试纸变蓝证明.
解答:
解:(1)氨气密度比空气轻,易溶于水,用向下排空气法收集,故答案为:向下排气集气;
(2)实验室制取氨气需要加热,与初中制取O2类似,;故答案为:O2;
(3)干燥氨气需要选择碱性干燥剂,故答案为:碱石灰;
(4)检验氨气是否已经收集满的方法,用一张湿润的红色石蕊试纸接近试管口,试纸变蓝说明已收集满,
故答案为:用一张湿润的红色石蕊试纸接近试管口,试纸变蓝说明已收集满.
(2)实验室制取氨气需要加热,与初中制取O2类似,;故答案为:O2;
(3)干燥氨气需要选择碱性干燥剂,故答案为:碱石灰;
(4)检验氨气是否已经收集满的方法,用一张湿润的红色石蕊试纸接近试管口,试纸变蓝说明已收集满,
故答案为:用一张湿润的红色石蕊试纸接近试管口,试纸变蓝说明已收集满.
点评:本题考查了实验室氨气的制备与收集,反应原理的分析判断,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
下列描述所对应的离子方程式正确的是( )
| A、钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ | ||||
| B、用CuCl2溶液做导电性实验,灯泡发光:CuCl2=Cu2++2Cl- | ||||
| C、铅蓄电池充电时的阳极反应:PbSO4+2H2O-2e-=PbO2+4H++SO42- | ||||
D、用铜做电极电解CuSO4溶液:2Cu2++2H2O
|
一定温度下,反应2SO2(g)+O2(g)?2SO3(g),达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4.缩小体积,反应再次达到平衡时,n(O2)=0.8mol,n(SO3)=1.4mol,此时SO2的物质的量应是( )
| A、0.4 mol |
| B、0.6 mol |
| C、0.8 mol |
| D、1.2 mol |
实验室制备氨气,检验是否收集满的正确方法是( )
| A、用手扇动收集的气体,有气味则已收集满 |
| B、将润湿的淀粉KI试纸接近瓶口,试纸变蓝则已收集满 |
| C、将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满 |
| D、用玻璃棒一端蘸取浓盐酸,接近瓶口,产生大量白烟,证明已收集满 |
下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A、酸性氧化物 二氧化碳 CO2 |
| B、酸 硫酸 H2S |
| C、碱性氧化物 氢氧化钙 Ca(OH)2 |
| D、碱 纯碱 NaOH |