题目内容
杭州一中化学学习小组对实验室用乙醇和浓硫酸加热来制备乙烯的反应进行探究,他们发现以下实验现象:
①反应过程中产生的气体有刺激性气味 ②反应后的溶液呈棕黑色
对此,他们猜测可能还有以下副反应:
C2H5OH+2H2SO4(浓)=2C+2SO2↑+5H2O C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
为了验证他们的猜想,他们将实验进行了如下改正,(如图所示)气体的流向做如下设计:A-B-C-D ①-E-F-G A-B-C-D②-H-I-K
三通管的作用是可以用止水夹夹住连接的橡皮管控制气体流向.
通过查资料得知,乙烯与酸性KmnO4溶液反应可以生成CO2.
他们实验的目的是通过下图设计的实验验证所有的可能产物(CO2、SO2、H2O、C2H4)
请你根据他们的设计完成下列问题:
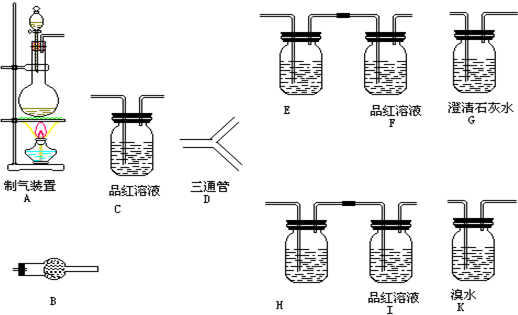
(1)装置A中缺少一种重要的仪器,这种仪器的作用为 .
(2)装置B中所装的试剂是 ,作用是 .
(3)装置C的作用是 .
(4)装置E中所装的试剂是 ,作用是 .
(5)装置H中所装的试剂是 ,作用是 .
(6)能够证明有CO2气体的现象是 .
(7)E中试剂与SO2反应的离子方程式为 .H中试剂与SO2反应的离子方程式为 .
①反应过程中产生的气体有刺激性气味 ②反应后的溶液呈棕黑色
对此,他们猜测可能还有以下副反应:
C2H5OH+2H2SO4(浓)=2C+2SO2↑+5H2O C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
为了验证他们的猜想,他们将实验进行了如下改正,(如图所示)气体的流向做如下设计:A-B-C-D ①-E-F-G A-B-C-D②-H-I-K
三通管的作用是可以用止水夹夹住连接的橡皮管控制气体流向.
通过查资料得知,乙烯与酸性KmnO4溶液反应可以生成CO2.
他们实验的目的是通过下图设计的实验验证所有的可能产物(CO2、SO2、H2O、C2H4)
请你根据他们的设计完成下列问题:

(1)装置A中缺少一种重要的仪器,这种仪器的作用为
(2)装置B中所装的试剂是
(3)装置C的作用是
(4)装置E中所装的试剂是
(5)装置H中所装的试剂是
(6)能够证明有CO2气体的现象是
(7)E中试剂与SO2反应的离子方程式为
考点:乙醇的消去反应
专题:实验题
分析:(1)用乙醇制取乙烯的反应中,需要用温度计控制反应温度;
(2)装置B用于检验混合气体中是否含有水分,可以用白色的无水硫酸铜检验;
(3)装置C中盛放的是品红溶液,用于检验混合气体中是否含有二氧化硫;
(4)①-E-F-G中,G为澄清石灰水,用于检验二氧化碳,则装置E的目的是除去混合气体中的乙烯和二氧化硫,避免干扰二氧化碳检验;
(5)装置K用于检验乙烯,则应该先将混合气体中的二氧化硫除去,所以装置H用于除去二氧化硫,可以使用氢氧化钠溶液;
(6)装置F用于检验二氧化硫是否除去,装置H用于检验二氧化碳,据此判断二氧化碳存在的现象;
(7)装置E中溴水与二氧化硫反应生成硫酸和溴化氢;装置H中氢氧化钠溶液与二氧化硫反应生成亚硫酸钠和水,据此写出反应的离子方程式.
(2)装置B用于检验混合气体中是否含有水分,可以用白色的无水硫酸铜检验;
(3)装置C中盛放的是品红溶液,用于检验混合气体中是否含有二氧化硫;
(4)①-E-F-G中,G为澄清石灰水,用于检验二氧化碳,则装置E的目的是除去混合气体中的乙烯和二氧化硫,避免干扰二氧化碳检验;
(5)装置K用于检验乙烯,则应该先将混合气体中的二氧化硫除去,所以装置H用于除去二氧化硫,可以使用氢氧化钠溶液;
(6)装置F用于检验二氧化硫是否除去,装置H用于检验二氧化碳,据此判断二氧化碳存在的现象;
(7)装置E中溴水与二氧化硫反应生成硫酸和溴化氢;装置H中氢氧化钠溶液与二氧化硫反应生成亚硫酸钠和水,据此写出反应的离子方程式.
解答:
解:(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,反应方程式为:CH3CH2OH
CH2=CH2↑+H2O,装置中缺少温度计,需要用温度计可知反应温度,
故答案为:控制反应温度;
(2)混合气体中可能含有CO2、SO2、H2O、C2H4,需要先用无水硫酸铜检验水蒸气,然后用品红溶液检验二氧化硫,所以装置B中盛放的是白色的无水硫酸铜,如果有水蒸气,则白色的无水硫酸铜变成蓝色,
故答案为:无水CuSO4;检验水蒸气;
(3)二氧化硫检验漂白性,能够使品红溶液褪色,所以装置C用于检验混合气体中是否含有二氧化硫,
故答案为:检验SO2;
(4)根据图示装置可知,G中盛放澄清石灰水,用于检验二氧化碳气体,用于二氧化硫也能够使澄清石灰水变浑浊,则应该先除去混合气体中的二氧化硫,所以装置H中盛放溴水,目的是除去SO2和C2H4,
故答案为:溴水; 除去SO2和C2H4;
(5)根据图示装置可知,装置K中溴水用于检验混合气体中的乙烯,用于二氧化硫也能够与溴水反应,则应该先除去混合气体中的二氧化硫,装置H中可以使用氢氧化钠溶液,
故答案为:NaOH溶液;除去SO2和CO2;
(6)检验混合气体中是否含有二氧化碳,则应该先判断混合气体中不含二氧化硫,然后用澄清石灰水检验,所以证明二氧化碳存在的现象为:F中品红不褪色,G中石灰水变浑浊,
故答案为:F中品红不褪色,G中石灰水变浑浊;
(7)装置E中溴水与二氧化硫反应生成硫酸和溴化氢,反应的离子方程式为:SO2+Br2+2H2O=SO42-+2Br-+4H+;
装置H中二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,反应的离子方程式为:SO2+2OH-=SO32-+H2O,
故答案为:SO2+Br2+2H2O=SO42-+2Br-+4H+;SO2+2OH-=SO32-+H2O.
| 浓硫酸 |
| 170℃ |
故答案为:控制反应温度;
(2)混合气体中可能含有CO2、SO2、H2O、C2H4,需要先用无水硫酸铜检验水蒸气,然后用品红溶液检验二氧化硫,所以装置B中盛放的是白色的无水硫酸铜,如果有水蒸气,则白色的无水硫酸铜变成蓝色,
故答案为:无水CuSO4;检验水蒸气;
(3)二氧化硫检验漂白性,能够使品红溶液褪色,所以装置C用于检验混合气体中是否含有二氧化硫,
故答案为:检验SO2;
(4)根据图示装置可知,G中盛放澄清石灰水,用于检验二氧化碳气体,用于二氧化硫也能够使澄清石灰水变浑浊,则应该先除去混合气体中的二氧化硫,所以装置H中盛放溴水,目的是除去SO2和C2H4,
故答案为:溴水; 除去SO2和C2H4;
(5)根据图示装置可知,装置K中溴水用于检验混合气体中的乙烯,用于二氧化硫也能够与溴水反应,则应该先除去混合气体中的二氧化硫,装置H中可以使用氢氧化钠溶液,
故答案为:NaOH溶液;除去SO2和CO2;
(6)检验混合气体中是否含有二氧化碳,则应该先判断混合气体中不含二氧化硫,然后用澄清石灰水检验,所以证明二氧化碳存在的现象为:F中品红不褪色,G中石灰水变浑浊,
故答案为:F中品红不褪色,G中石灰水变浑浊;
(7)装置E中溴水与二氧化硫反应生成硫酸和溴化氢,反应的离子方程式为:SO2+Br2+2H2O=SO42-+2Br-+4H+;
装置H中二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,反应的离子方程式为:SO2+2OH-=SO32-+H2O,
故答案为:SO2+Br2+2H2O=SO42-+2Br-+4H+;SO2+2OH-=SO32-+H2O.
点评:本题考查了乙醇的消去反应的实验,题目难度中等,试题题量较大,知识点较多,综合性较强,注意掌握乙醇、乙烯的化学性质,明确乙烯的检验方法,试题充分考查了学生的分析、理解能力及化学实验能力.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
检验试样中某离子的操作及结论合理的是( )
| A、先加BaCl2溶液有白色沉淀,再加稀HNO3溶液不溶解,则试样中一定有SO42- |
| B、加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,则试样中一定有CO32- |
| C、加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,则试样中一定有NH4+ |
| D、透过蓝色钴玻璃观察到焰色为紫色,则试样中一定有钾元素、没有钠元素 |
在一定条件下,在容积为2L的密闭容器中,将2mol 气体M和3mol N气体混合,发生如下反应:2M(g)+3N(g)?x Q(g)+3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4mol/L,下列有关叙述正确的是( )
| A、x值为2 |
| B、混合气体的密度增大 |
| C、平衡时N的浓度为0.3 mol/L |
| D、N的转化率为20% |
铁丝、铜片在氯气中燃烧的烟的颜色分别为( )
| A、棕黄、棕红 |
| B、棕黄、苍白 |
| C、棕红、苍白 |
| D、棕红、棕黄 |
和下列离子反应方程式相对应的化学方程式正确的是( )
| A、Zn2++2OH-=Zn(OH)2↓ ZnCO3+2NaOH=Zn(OH)2↓+Na2CO3 |
| B、Ba2++SO42-=BaSO4↓ Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C、Ag++Cl-=AgCl↓ AgNO3+NaCl=AgCl↓+NaNO3 |
| D、Cu+2Ag+=Cu2++2Ag↓ Cu+2AgCl=2Ag+CuCl2 |
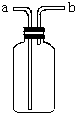 如图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其他用途:
如图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其他用途:
