题目内容
下列溶液:①CH3COOH ②H2SO4 ③HCl ④Ba(OH)2 ⑤NaOH⑥CH3COONa ⑦KCl ⑧NH4Cl其物质的量浓度均为0.1mol/L,pH由小到大排列顺序为( )
| A、②③①⑧⑦⑥⑤④ | B、④⑤⑥⑦⑧①③② | C、③②①⑥⑦⑧④⑤ | D、②③①⑤④⑧⑦⑥ |
分析:先将物质的按照碱、盐、酸的顺序分类,再根据盐的水解和弱电解质的电离特点比较PH,再按照溶液的PH由大到小进行排序.
解答:解:属于碱的为:④Ba(OH)2⑤NaOH,浓度相同时,碱性④>⑤;
水解呈碱性的为:⑥CH3COONa,但水解程度较小,则pH:④>⑤>⑥;
溶液呈中性的为:⑦KCl;
溶液呈酸性的有:①②③⑧,其中①为一元弱酸,②为二元强酸,③为一元强酸,⑧水解呈酸性,浓度相同时,
溶液的pH:②<③<①<⑧,
综合以上分析可知,溶液的pH由小到大的顺序是为:②③①⑧⑦⑥⑤④,
故选A.
水解呈碱性的为:⑥CH3COONa,但水解程度较小,则pH:④>⑤>⑥;
溶液呈中性的为:⑦KCl;
溶液呈酸性的有:①②③⑧,其中①为一元弱酸,②为二元强酸,③为一元强酸,⑧水解呈酸性,浓度相同时,
溶液的pH:②<③<①<⑧,
综合以上分析可知,溶液的pH由小到大的顺序是为:②③①⑧⑦⑥⑤④,
故选A.
点评:本题考查了溶液PH的大小比较,题目难度不大,注意考虑电解质的强弱以及盐类的水解情况,试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
 如图所示为不饱和烃加氢时的能量变化示意图,具体数据如下: 如图所示为不饱和烃加氢时的能量变化示意图,具体数据如下:
|
下列物质中,既不能使溴的四氯化碳溶液褪色,也不能使酸性高锰酸钾溶液褪色的是( )
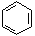
①C5H12 ②CH3C≡CCH3 ③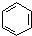 ④
④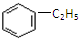 ⑤CH2=CH2 ⑥
⑤CH2=CH2 ⑥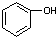
①C5H12 ②CH3C≡CCH3 ③
 ④
④ ⑤CH2=CH2 ⑥
⑤CH2=CH2 ⑥
| A、①③④ | B、②⑤⑥ | C、①④⑤ | D、①③ |
下列物质中,既不能使溴的四氯化碳溶液褪色,也不能使酸性高锰酸钾溶液褪色的是
①C5H12 ②CH3C≡CCH3 ③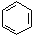 ④
④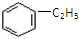 ⑤CH2=CH2 ⑥
⑤CH2=CH2 ⑥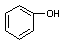
| A.①③④ | B.②⑤⑥ | C.①④⑤ | D.①③ |
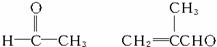
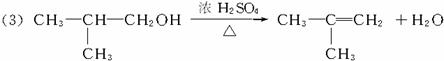
 ④
④