题目内容
19.下列有关NaHSO3溶液的叙述正确的是( )| A. | 该溶液中K+、Ca2+、ClO-、Br-可以大量共存 | |
| B. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具漂白性 | |
| C. | NaHSO3溶液c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-) | |
| D. | 和足量Ca(OH)2溶液反应的离子方程式:Ca2++OH-+HSO3-=CaSO3↓+H2O |
分析 A.ClO-与HSO3-发生氧化还原反应;
B.能使含I2的淀粉溶液蓝色褪去,可知碘与NaHSO3发生氧化还原反应;
C.溶液中遵循电荷守恒;
D.NaHSO3完全反应,生成亚硫酸钙、水、NaOH.
解答 解:A.ClO-与HSO3-发生氧化还原反应,不能大量共存,故A错误;
B.能使含I2的淀粉溶液蓝色褪去,可知碘与NaHSO3发生氧化还原反应,说明NaHSO3溶液具有还原性,故B错误;
C.溶液中遵循电荷守恒,则电荷守恒式为c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-),故C错误;
D.NaHSO3完全反应,生成亚硫酸钙、水、NaOH,离子反应为Ca2++OH-+HSO3-=CaSO3↓+H2O,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重氧化还原反应、与量有关的离子共存考查,题目难度不大.

练习册系列答案
相关题目
9.硅被誉为无机非金属材料的主角.下列物品用到硅单质的是( )
| A. | 玻璃制品 | B. | 石英钟表 | C. | 计算机芯片 | D. | 光导纤维 |
10.对合金的性质或应用,下列说法不正确的是( )
| A. | 合金的硬度一般比它的各成分金属的小,多数合金的熔点一般也比它的各成分金属的高 | |
| B. | 合金在工业上具有比纯金属更广泛的用途 | |
| C. | 制饭勺、饭盒、高压锅等的不锈钢是合金 | |
| D. | 青铜是我国使用最早的合金 |
7.下列离子方程式书写正确的是( )
| A. | 钠与水的反应 Na+H2O═OH-+H2↑ | |
| B. | NaHCO3溶液与盐酸的反应 CO32-+2H+═H2O+CO2↑ | |
| C. | 用FeCl3溶液腐蚀铜线路板 Cu+Fe3+═Cu2++Fe2+ | |
| D. | AlCl3溶液中加入过量氢氧化钠溶液 Al3++4OH-═AlO2-+2H2O |
14.常温下,下列溶液中可能大量共存的离子组是( )
| A. | 水电离产生的c(H+)=1×10-12mol•L-1的溶液:Mg2+、SO42-、NO3-、Cl- | |
| B. | 含有大量Fe3+的溶液:K+、Na+、AlO2-、SO42- | |
| C. | 能使pH试纸变红的溶液:NH4+、Na+、NO3-、HCO3- | |
| D. | 含有大量S2-的溶液:Na+、ClO-、Cl-、CO32- |
4.下列化学用语的理解正确的是( )
| A. | 电子式: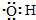 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| B. | 离子结构示意图: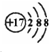 可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- | |
| C. | 比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 聚丙烯的结构简式: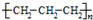 |
11.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释正确的是 ( )
| 现象 | 解释 | |
| A | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
| B | SO2能使酸性高锰酸钾溶液褪色 | SO2具有还原性 |
| C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| D | 铁与稀硝酸反应有气泡产生 | 铁与稀硝酸发生了置换反应 |
| A. | A | B. | B | C. | C | D. | D |
8.我国是世界上缺铁性贫血发生率较高的国家之一,2004年我国政府就已经启动了铁强化酱油项目,推广铁强化酱油.这里的铁是指( )
| A. | 元素 | B. | 单质 | C. | 原子 | D. | 分子 |
9.CH3COOH与CH3COONa浓度均为0.1mol•L-1的混合溶液中,离子浓度由大到小的顺序是( )
| A. | c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | B. | c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | ||
| C. | c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | D. | c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |