题目内容
15.下列名词中,哪个名词不属于物理量( )| A. | 长度 | B. | 气体摩尔体积 | C. | 摩尔 | D. | 摩尔质量 |
分析 国际单位制中的七个基本物理量及其单位为:长度 米(m);质量 千克(kg);时间 秒(s);电流 安培(A);热力学温度 开尔文(K);发光强度 坎德拉(cd);物质的量 摩尔(mol).据此即可解答.
解答 解:A.长度是国际单位制中的七个基本物理量之一,表示物体或线段长短的程度,故A正确;
B.气体摩尔体积是物理量,表示单位物质的量的物质所占体积,故B正确;
C.物质的量的单位是摩尔,摩尔是其单位,不属于国际单位制中的七个基本物理量之一,故C错误;
D.摩尔质量是基本物理量之一,表示单位物质的量的物质具有的质量,故D正确;
故选C.
点评 本题考查了基本物理量的掌握情况,注意物质的量是国际单位制中的七个基本物理量之一,摩尔是其单位,比较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.将铁粉和铜粉的混合物投入一定量的稀盐酸中,铁粉和铜粉仍有剩余,向反应后的溶液中缓缓地通入氯气.反应分成以下几个阶段:
回答以下问题:
(1)写出第一阶段可能发生的离子反应方程式Fe+2H+=Fe2++H2↑.
(2)第三阶段金属粉末是否有残留可能有.选填(“一定有”、“一定没有”、“可能有”)
(3)第三阶段发生的离子反应方程式是2Fe2++Cl2=2Cl-+Fe3+,2Fe3++Cu=Cu2++2Fe2+(和以上(1)中重复的不写).
(4)第四阶段金属粉末是否有残留?一定没有.选填(“一定有”、“一定没有”、“可能有”)
(5)第五阶段溶液中存在的金属阳离子是Fe3+、Fe2+、Cu2+(写出离子符号).
| 反应阶段 | 溶液中的存在的金属离子 | 残留的金属粉末 | 发生的离子反应 |
| 第一阶段 | 只有一种 | 有两种 | (1) |
| 第二阶段 | 只有一种 | 只有一种 | |
| 第三阶段 | 只有两种 | (2) | (3) |
| 笫四阶段 | 有三种 | (4) | |
| 笫五阶段 | (5) |
(1)写出第一阶段可能发生的离子反应方程式Fe+2H+=Fe2++H2↑.
(2)第三阶段金属粉末是否有残留可能有.选填(“一定有”、“一定没有”、“可能有”)
(3)第三阶段发生的离子反应方程式是2Fe2++Cl2=2Cl-+Fe3+,2Fe3++Cu=Cu2++2Fe2+(和以上(1)中重复的不写).
(4)第四阶段金属粉末是否有残留?一定没有.选填(“一定有”、“一定没有”、“可能有”)
(5)第五阶段溶液中存在的金属阳离子是Fe3+、Fe2+、Cu2+(写出离子符号).
10.下列说法中,正确的是( )
| A. | 气体的摩尔体积为22.4 L•mol-12 | |
| B. | 1 mol H2的质量是2 g,它所占的体积是22.4 L | |
| C. | 在标准状况下,1 mol任何气体所占的体积都为22.4 L•mol-1 | |
| D. | 在标准状况下,1 mol任何气体所占的体积都约为22.4 L |
20.下列溶液:①硝酸钡溶液 ②碘水 ③酸性高锰酸钾溶液 ④氯化铁溶液 ⑤品红溶液,其中能用来区别SO2和CO2气体的是( )
| A. | ③⑤ | B. | ②③⑤ | C. | ①②③⑤ | D. | ①②③④⑤ |
7.下式表示一种有机物的结构,关于它的性质叙述中不正确的是( )
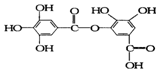

| A. | 它能与纯碱溶液反应 | |
| B. | 它可以水解,水解生成的有机产物有二种 | |
| C. | 1 mol该有机物最多能和8 mol NaOH反应 | |
| D. | 该有机物能发生取代反应 |
4.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 沉淀溶解后,将会生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| C. | 向反应后的溶液加入乙醇,溶液不会有变化,因为[Cu(NH3)4]2+不会与乙醇发生反应 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
5.化学基本概念及原理在化学反应中应用广泛.
(1)甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,反应如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 K1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
③CO(g)+2H2(g)?CH3OH(g)△H3 K3
已知相关的化学键键能(E)数据如表:
已知△H2=+41kJ•mol-1,则△H3=-220kJ•mol-1;平衡常数K3=$\frac{{K}_{1}}{{K}_{2}}$(用K1、K2表示).
(2)NaAlH4是重要的还原剂和储氢材料.可由甲合成NaAlH4,加热7.20g甲至完全分解,得到金属钠和3.36L(标准状况)的H2.
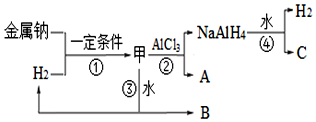
①A的电子式为Na+[:H]-;反应③的化学方程式为NaH+H2O=H2↑+NaOH.
②NaAlH4在催化剂作用下释放氢时生成Na3AlH6和两种单质,则该反应的化学方程式为3NaAlH4=Na3AlH6+3H2↑+2Al.
③为制备甲并检验其是否纯净,某同学设计方案:用惰性气体赶尽反应体系中的空气,将锌和稀硫酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质;取该固体物质与水反应,产生H2,证明固体物质一定是纯净的.该同学设计的方案是否合理并说明理由不合理,Na和NaH都能与水反应生成H2.
(1)甲醇是重要的化工原料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,反应如下:
①CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1 K1
②CO2(g)+H2(g)?CO(g)+H2O(g)△H2 K2
③CO(g)+2H2(g)?CH3OH(g)△H3 K3
已知相关的化学键键能(E)数据如表:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 745 | 465 | 413 |
(2)NaAlH4是重要的还原剂和储氢材料.可由甲合成NaAlH4,加热7.20g甲至完全分解,得到金属钠和3.36L(标准状况)的H2.

①A的电子式为Na+[:H]-;反应③的化学方程式为NaH+H2O=H2↑+NaOH.
②NaAlH4在催化剂作用下释放氢时生成Na3AlH6和两种单质,则该反应的化学方程式为3NaAlH4=Na3AlH6+3H2↑+2Al.
③为制备甲并检验其是否纯净,某同学设计方案:用惰性气体赶尽反应体系中的空气,将锌和稀硫酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质;取该固体物质与水反应,产生H2,证明固体物质一定是纯净的.该同学设计的方案是否合理并说明理由不合理,Na和NaH都能与水反应生成H2.