题目内容
氨气催化氧化生产硝酸,硝酸厂常用催化还原法处理尾气:催化剂存在时用H2将NO2还原为N2.
已知:2H2( g )+O2( g )=2H2O ( g )△H=-483.6kJ/molN2( g )+2O2( g )=2NO2 ( g )△H=+67.7kJ/mol则反应4H2( g )+2NO2 ( g )=N2( g )+4H2O ( g ) 的反应热△H= .
已知:2H2( g )+O2( g )=2H2O ( g )△H=-483.6kJ/molN2( g )+2O2( g )=2NO2 ( g )△H=+67.7kJ/mol则反应4H2( g )+2NO2 ( g )=N2( g )+4H2O ( g ) 的反应热△H=
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol ①
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol ②
由盖斯定律将①×2-②可得热化学方程式.
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol ②
由盖斯定律将①×2-②可得热化学方程式.
解答:
解:已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol ①
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol ②
由盖斯定律可知,①×2-②得4H2(g)+2NO2(g)=N2(g)+4H2O(g),
故△H=2×(-483.6kJ/mol)-67.7kJ/mol=-1034.9kJ/mol,
故热化学方程式为:4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1034.9kJ/mol,
故答案为:-1034.9kJ/mol.
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol ②
由盖斯定律可知,①×2-②得4H2(g)+2NO2(g)=N2(g)+4H2O(g),
故△H=2×(-483.6kJ/mol)-67.7kJ/mol=-1034.9kJ/mol,
故热化学方程式为:4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1034.9kJ/mol,
故答案为:-1034.9kJ/mol.
点评:本题考查了反应热的计算,掌握盖斯定律的运用是解答关键,题目难度不大.

练习册系列答案
相关题目
下列方法中,不能用于实验室制备氨气的是( )
| A、加热浓氨水 |
| B、将浓氨水滴到生石灰上 |
| C、加热氯化铵固体 |
| D、将熟石灰和氯化铵的混合物加热 |
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
| A、加入KSCN溶液一定不变红色 |
| B、溶液中一定含Fe2+ |
| C、溶液中一定不含Cu2+ |
| D、剩余固体中一定含Cu |
下列物质中属于强电解质的是( )
| A、NH3?H2O |
| B、三氧化硫 |
| C、醋酸钠 |
| D、食盐水 |
下列两种情况下:①2g CO和2g H2混合②3g CO和1g H2混合,之后在足量氧气中充分燃烧,生成的气体与Na2O2固体(足量)反应,Na2O2固体的质量增加关系为( )
| A、①=② | B、①<② |
| C、①>② | D、无法判断 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,11.2 L乙烯含有的极性共价键数为NA |
| B、常温下,5.6 L NO和5.6 L O2的混合气体中含有的分子数为0.5NA |
| C、16.9 g BaO2固体中阴、阳离子总数为0.2NA |
| D、含有1 mol Fe(OH)3的氢氧化铁胶体中含有胶粒数为NA |
下列物质的保存方法正确的是( )
| A、钠保存在盛有水的试剂瓶中 |
| B、漂白粉露置于空气中 |
| C、浓硝酸保存在棕色玻璃瓶中 |
| D、氢氧化钠溶液保存在带玻璃塞的玻璃瓶中 |
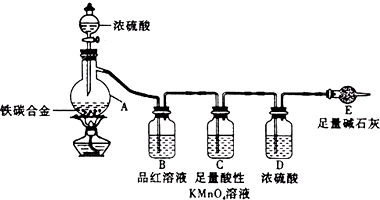 某校化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题.Ⅰ探究浓硫酸的某些性质
某校化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题.Ⅰ探究浓硫酸的某些性质