题目内容
8.向炭粉、Cu和Fe2O3组成的混合粉末中加入一定量的稀硫酸,充分反应后过滤,得到溶液A,将沉淀物洗涤、干燥,得到固体B.(1)溶液A中一定存在的金属阳离子是Fe2+、Cu2+.
(2)写出相关的离子方程式Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+.
分析 (1)当铜过量或恰好与铁离子反应时,此时溶液A中不含有Fe3+,一定含有Fe2+、Cu2+;当铜不足时,铜完全反应后Fe3+有剩余,则A溶液中含有金属离子为:Fe3+、Fe2+、Cu2+;
(2)氧化铁和盐酸反应生成氯化铁和水,氯化铁和铜反应生成氯化亚铁和氯化铜;
解答 解:(1)当铜过量或恰好与铁离子反应时,此时溶液A中不含有Fe3+,一定含有Fe2+、Cu2+;当铜不足时,铜完全反应后Fe3+有剩余,则A溶液中含有金属离子为:Fe3+、Fe2+、Cu2+,所以A溶液中一定含有的金属阳离子为:Fe2+、Cu2+,
故答案为:Fe2+、Cu2+;
(2)氧化铁和盐酸反应生成氯化铁和水,反应的离子方程式为;Fe2O3+6H+=2Fe3++3H2O,氯化铁和铜反应生成氯化亚铁和氯化铜,反应的离子方程式为:Cu+2Fe3+=2Fe2++Cu2+,
故答案为:Fe2O3+6H+=2Fe3++3H2O、Cu+2Fe3+=2Fe2++Cu2+.
点评 本题考查了离子反应及其应用,题目难度中等,明确发生的反应实质为解答关键,注意掌握离子反应发生条件及离子共存的判断方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
4.用铝片与稀硫酸反应制取氢气时,下列措施一定能使氢气生成速率加大的是( )
| A. | 不用铝片,改用铝粉 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 不用稀硫酸,改用浓硝酸 | D. | 加入少量稀盐酸 |
19.为提纯下列物质(括号中为杂质),选用的试剂和分离方法都正确的是( )
| 物质 | 除杂试剂 | 分离方法 | |
| A | 碳酸氢钠(碳酸钠) | - | 加热 |
| B | 二氧化碳(氯化氢) | 饱和Na2CO3 | 洗气 |
| C | 乙醇(水) | 生石灰 | 蒸馏 |
| D | 氧化铁(氧化铝) | NaOH溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.用一种试剂就可以将NaOH、KSCN、AgNO3、Na2SO4四种无色溶液一一鉴别出来,这种试剂是( )
| A. | 稀盐酸 | B. | FeCl3 | C. | Fe(NO3)3 | D. | BaCl2 |
13.下列表示物质的化学式可以称为分子式的是( )
| A. | SiO2 | B. | CO2 | C. | Cu | D. | KOH |
20.已知下列两个热化学方程式:2H2(g)+O2(g)→2H2O(l)+571.6kJ,C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)+2220.0kJ.实验测得,H2和C3H8的混合气体共10mol,完全燃烧放热7694kJ,则混合气体中H2和C3H8的体积比是( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |
17.3mol Cl2和3mol NO相比较,下列叙述中正确的是( )
| A. | 分子数相等 | B. | 原子数相等 | C. | 体积相等 | D. | 质量相等 |
18.下列单质或化合物性质的描述正确的是( )
| A. | NaHSO4水溶液显中性 | |
| B. | NO2溶于水时发生氧化还原反应 | |
| C. | SiO2与酸、碱均不反应 | |
| D. | Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
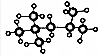 ,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;
,其分子式为:C8H18,A的一氯代物有4种;A有多种同分异构体,写出其中一氯代物只有一种同分异构体的结构简式(CH3)3CC(CH3)3;